 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电势滴定时,由于在计量点附近离子浓度发生______,引起指示电极的______发生突跃,故测量工作电池的______变
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“电势滴定时,由于在计量点附近离子浓度发生______,引起指…”相关的问题
更多“电势滴定时,由于在计量点附近离子浓度发生______,引起指…”相关的问题
某弱酸
已知下列元素电势图:
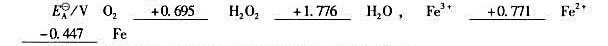
①H202能否发生歧化反应?如果能发生,写出反应式。
②在pH=3的条件下,判断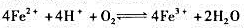 进行的方向。(设其他各离子浓度为1.0mol/L)。
进行的方向。(设其他各离子浓度为1.0mol/L)。
③计算298K时,反应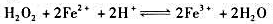 的平衡常数。(用
的平衡常数。(用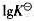 表示)
表示)
计算pH=10.0,在总浓度为0.1mol·L-1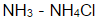 缓冲溶液中,Ag+/Ag电对的条件电势。忽略离子强度及形成
缓冲溶液中,Ag+/Ag电对的条件电势。忽略离子强度及形成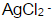 络合物的影响。(Ag-NH3络合物的lgβ1~lgβ2分别为3.24、7.05;
络合物的影响。(Ag-NH3络合物的lgβ1~lgβ2分别为3.24、7.05;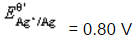 。)
。)
在298 K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0. 01 mol·kg-1)和CuCl2(0.02 mol·kg-1)的水溶液。若电解过程中超电势可忽略不计,试问(设活度因子均为1):(1)何种金属先在阴极析出? (2) 第二种金属析出时,至少须加多少电压? (3) 当第二种金属析出时,第一种金属离子在溶液中的浓度?(4)事实上O2(g)在石墨上是有超电势的,若设超电势为0.85V,则阳极上首先应发生什么反应?
在pH=5.5的缓冲介质中,以0.010 mol·L-1EDTA滴定20.00mL同浓度的金属离子M2+至终点。已知在此条件下终点误差为0.1%,当加入19.98~20.02mLEDTA时(即化学计量点前后0.1%),pM改变1个单位。计算稳定常数KMY为多少?(pH=5.5时,lgαY(H)=5.5)
计算在1,10-邻二氮菲存在下,溶液含H2SO4浓度为1mol.L-1时,Fe3+/Fe2+电对的条件电势。(忽略离子强度的影响。已知在1mol·L-1H2SO4溶液中,亚铁络合物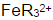 与高铁络合物
与高铁络合物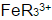 的稳定常数之比KⅡ/KⅢ=2.8×106。)
的稳定常数之比KⅡ/KⅢ=2.8×106。)