 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某研究小组以紫葡萄为原料制作葡萄酒,实验中,判断发酵完毕的依据是()
A.发酵瓶中pH开始下降
B.发酵瓶中停止出现气泡
C.发酵瓶中酒精浓度达到30%
D.发酵瓶中酵母菌数量急剧减少
 答案
答案
B、发酵瓶中停止出现气泡
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.发酵瓶中pH开始下降
B.发酵瓶中停止出现气泡
C.发酵瓶中酒精浓度达到30%
D.发酵瓶中酵母菌数量急剧减少
 答案
答案
B、发酵瓶中停止出现气泡
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某研究小组以紫葡萄为原料制作葡萄酒,实验中,判断发酵完毕的依…”相关的问题
更多“某研究小组以紫葡萄为原料制作葡萄酒,实验中,判断发酵完毕的依…”相关的问题
A.红葡萄酒是用青葡萄或紫葡萄去皮后再压榨取汁,经过自然发酵而成
B.白葡萄酒是用紫葡萄连皮一起压榨取汁,经过自然发酵而成
C.将紫青葡萄混合在一起榨汁发酵可以制成玫瑰葡萄酒
D.酿造香槟酒的原料有紫葡萄.白葡萄.以紫葡萄为主
E.在酿制白葡萄酒中浸入紫葡萄皮可以制成玫瑰葡萄酒
工业上以氨气为原料制备硝酸的过程如下: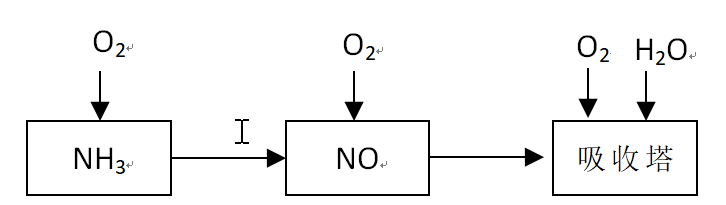 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。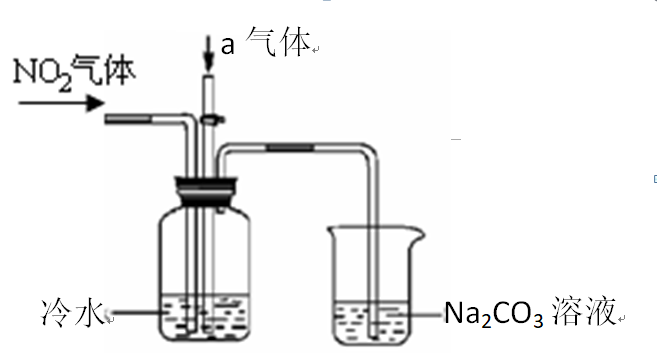
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
A.利用沸点不同蒸馏提纯该有机物
B.利用核磁共振氢谱确定该有机物的相对分子质量为46
C.利用燃烧法确定该有机物的实验式为C2H6O
D.利用红外光谱图确定该有机物分子中含O—H键
A.实验编号离子加入量/(mg•L-1)分解率/%
B.①无—2
C.②
A.将水温都控制在20℃
B.两组都用河水
C.将鱼卵数减少到10个
D.将水减少到1000mL
A.白化病,在学校内随机抽样调查
B.红绿色盲,在患者家系中调查
C.软骨发育不全,在市中心随机抽样调查
D.糖尿病,在患者家系中随机调查
某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原Cu0呢?他们设计实验制取氮气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式()。
(2有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的()(填“能”或“否”)。理由是()。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性: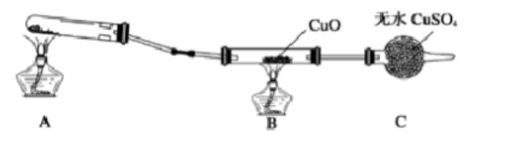 ⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
(2)利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与Cu0反应的化学方程式()。
(三)问题讨论:
有同学认为:NH3与Cu0反应生成的红色物质中可能含有Cu20.已知:Cu20是一种碱性氧化物;在酸性溶液中,Cu'的稳定性差(Cu+→Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu0:()。