 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
若键轴为z轴,下列2个原子轨道重叠不能形成σ键的是()。
A.s-s
B.s-pz
C.px-px
D.pz-pz
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.s-s
B.s-pz
C.px-px
D.pz-pz
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若键轴为z轴,下列2个原子轨道重叠不能形成σ键的是()。”相关的问题
更多“若键轴为z轴,下列2个原子轨道重叠不能形成σ键的是()。”相关的问题
某晶系属于立方晶系,一晶面截χ轴于
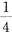 ,y轴于
,y轴于
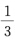 b,z轴于
b,z轴于
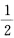 c,则该晶面的指标为()。
c,则该晶面的指标为()。
A.(364)
B.(234)
C.(21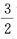 )
)
D.(468)
A.原子轨道的杂化,只有在形成分子的过程中才会发生,而孤立的原子是不可能发生杂化的
B.只有能量相近的原子轨道才能发生杂化
C.一定数目的原子轨道杂化后,可以得到更多数量的杂化轨道
D.CH4分子中有四个能量相等的C—H键,键角为109°28′,分子的空间构型为正四面体,这一情况可以用杂化轨道理论解释