 更多“在实际工作中运用问题界定思维,对“猜你喜欢”问题进行界定时,…”相关的问题
更多“在实际工作中运用问题界定思维,对“猜你喜欢”问题进行界定时,…”相关的问题
A.我不知道这件事是谁做的,但我猜做这件事的人一定对我们的情况比较熟悉
B.老师告诉我们:他对我们严,是宁愿欠我们一个轻松愉快的初三,也不愿我们中考后低头哭泣
C.谢谢老师,企业家说:是你们的帮助,才有今天的我
D.是让你的生命更加朝气勃勃还是让暮气滋长而举步不前这拷问着人生的选择
A.科学决策
B.科学监管
C.科学治理
D.科学追责
随着工业的迅速发展,产生的废水对水体的污染也日趋严重。通过控制溶液的pH对工业废水中的金属离子进行别离是实际工作中经常使用的方法。下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5mol•L-1时通常认为该离子沉淀完全)。 问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题二、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准
①Cr2O72-转变为Cr3+的离子方程式为()。
②pH对废水中Cr2072-去除率的影响如右图。你认为电解过程中溶液的pH取值在()范围内对降低废水中的铬含量最有利,请说明理由:()。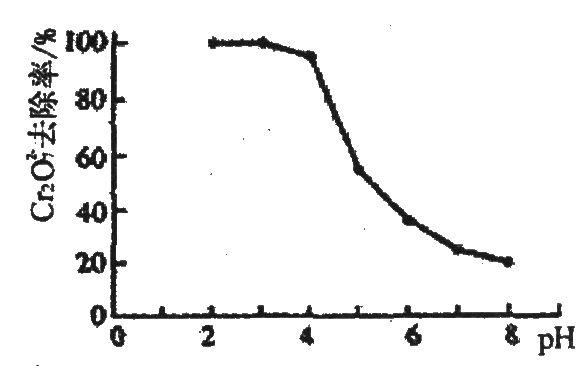
问题三、沉淀转化在生产中也有重要应用。例如,用Na2C03溶液可以将锅炉水垢中的CaS04转化为较疏松而易清除的CaC03,该沉淀转化到达平衡时,其平衡常数K=()。(已知Ksp(CaS04)=9.1x10-6,Ksp(CaC03)=2.8x10-9)
A.在实际工作中既要认识事物间的区别,又要认识事物间的联系
B.要在对立把握统一
C.有差别的地方没有统一,有统一的地方没有差别
D.只有在绝对统一中思维
A.戈登技术
B.头脑风暴法
C.联想型思维
D.收敛式思维


 如果结果不匹配,请
如果结果不匹配,请 

















