 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在298K和标准状态时,下列反应均为非自发反应,其中在高温时仍为非自发的反应是( )。
在298K和标准状态时,下列反应均为非自发反应,其中在高温时仍为非自发的反应是()。
A.Ag2O(s)=2Ag(s)+ O2(g)
O2(g)
B.N2O2=2NO2(g)
C.6C(s)+6H2O(g)=C6H12O6(s)
D.Fe2O3(s)+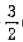 C(s)=2Fe(s)+
C(s)=2Fe(s)+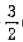 CO2g
CO2g
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在298K和标准状态时,下列反应均为非自发反应,其中在高温时…”相关的问题
更多“在298K和标准状态时,下列反应均为非自发反应,其中在高温时…”相关的问题
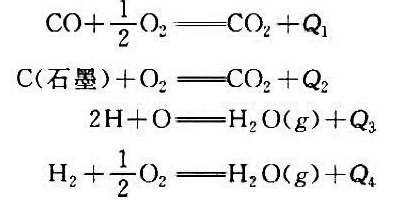
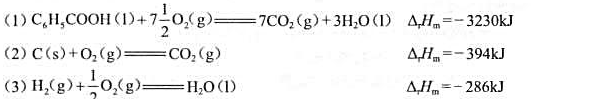 求C6H5COOH(1)的标准生成热ΔHƟm。
求C6H5COOH(1)的标准生成热ΔHƟm。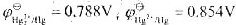 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。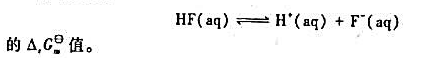
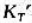
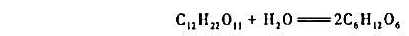
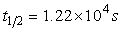 ,且
,且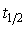 与反应物浓度无关。
与反应物浓度无关。
















