 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知,则反应的平衡常数为 (A) 4.52×106 (B) 2.21×10-7 (C) 31.8 (D) 0.707
已知
 的平衡常数为
的平衡常数为
(A) 4.52×106(B) 2.21×10-7(C) 31.8 (D) 0.707
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知
 的平衡常数为
的平衡常数为
(A) 4.52×106(B) 2.21×10-7(C) 31.8 (D) 0.707
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知,则反应的平衡常数为 (A) 4.52×106 (B) …”相关的问题
更多“已知,则反应的平衡常数为 (A) 4.52×106 (B) …”相关的问题
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
已知:Kspθ(Ag2 CrO4)=1.1×10-12,Kspθ(PbCrO4)=2.8×10-13,Kspθ(PbI2)=7.1×10-9,Kspθ(CaCrO4)=7.1×10-4,若向Ag+,Pb2+,Ca2+的浓度均为0.1 mol.dm-3的混合溶液中滴加K2CrO4溶液,则出现沉淀的顺序为________________;若将PbCrO4沉淀转化为PbI2沉淀,转化方程式为________________,转化反应的平衡常数Kθ= ________________。
298K时,已知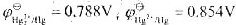 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
A.20
B.0.02
C.0.05
D.无法确定
A.Kp① >Kp②
B.Kp①
C.Kp①=Kp②
D.无法确定
A.HF的电离平衡常数为7.2×10−4
B.HNO2的电离平衡常数为4.9×10−10
C.根据①③两个反应即可知三种酸的相对强弱
D.HNO2的电离平衡常数比HCN大,比HF小
在温度为700℃时,有反应:
(1)

(2)

则反应 的平衡常数为
的平衡常数为