 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
体积相等的0.1mol·dm-3甲酸溶液的pH值为4.30,则甲酸的解离度为0.5%。()
体积相等的0.1mol·dm-3甲酸溶液的pH值为4.30,则甲酸的解离度为0.5%。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
体积相等的0.1mol·dm-3甲酸溶液的pH值为4.30,则甲酸的解离度为0.5%。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“体积相等的0.1mol·dm-3甲酸溶液的pH值为4.30,…”相关的问题
更多“体积相等的0.1mol·dm-3甲酸溶液的pH值为4.30,…”相关的问题
下列各溶液浓度均为0.1mol·dm-3,按pH从小到大顺序排列
KCN NH4F NH4Ac NH4NO3Na2CO3
试用近似计算说明,在0.10mol·dm-3的HAc溶液中通入H2S达饱和(约0.1mol·dm-3H2S),能否使溶液中0.10mol·dm-3的Mn2+以MnS形式沉淀出来?(已知K(HAc)=1.8×10-5,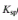 (MnS)=1.4×10-15,H2S的K1=1.32×10-7,K2=7.10×10-15)
(MnS)=1.4×10-15,H2S的K1=1.32×10-7,K2=7.10×10-15)
A.大于-0.06V
B.-0.06V
C.小于-0.06V
D.不能判定
刚果红溶液100mL,浓度为0.1mol·dm-3,按下式全部解离
NaR→Na++R-
若将它放在一半透膜做的袋内与100mL水达成平衡,试计算膜两边的pH值和膜电位。
A.25:1
B.1:25
C.40:1
D.1:40
某电导池装有电导率为0.141S·m-1的KCI水溶液,在25℃时测得电阻是525Ω,在同一电导池中装入0.1mol·dm-3的NH3·H2O溶液,测得其电阻是2030Ω,计算NH3·H2O的解离度和标准解离平衡常数。
298K时,在某一电导池中充以0.1mol·dm-1、电导率为0.14114S·m-1的KCl溶液,测得其电阻为525Ω。当在该电导池内充以0.10mol·dm-3的NH3·H2O溶液时,测得其电阻为2030Ω,已知此时所用水的电导率为2×10-4S·m-1。试求:
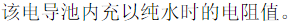
A.向Na2CO3溶液中加入甲酸有气泡产生
B.向碳酸中加入NaHCO3固体,c(H+)减小
C.向0.1mol/L甲酸中加入蒸馏水,c(H+)减小
D.25℃时,向甲酸中加入NaOH溶液,HCOOH的电离程度和Ka均增大