 更多“下列分子中,以sp3不等性杂化轨道成键的是()”相关的问题
更多“下列分子中,以sp3不等性杂化轨道成键的是()”相关的问题
第1题
下列关于共价键的说法中,错误的是()。
A.N2分子包含一个s键和两个π键
B.CO分子中存在配位键
C.原子形成共价键时必须遵守饱和性和方向性原则
D.sp2杂化轨道是由1s和2p轨道杂化而成
第2题
试用价层电子对互斥理论判断下列分子或离子的空间构型,再用杂化轨道理论说明它们的成键情况。(1
试用价层电子对互斥理论判断下列分子或离子的空间构型,再用杂化轨道理论说明它们的成键情况。(1
点击查看答案
试用价层电子对互斥理论判断下列分子或离子的空间构型,再用杂化轨道理论说明它们的成键情况。
(1)SF3; (2)BeF3; (3)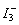 ; (4)
; (4)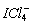 ;
;
第3题
已知下列分子的几何构型,试用杂化轨道理论分析它们的成键情况: (1)PCI5三角锥;(2)SiF4⌘
已知下列分子的几何构型,试用杂化轨道理论分析它们的成键情况: (1)PCI5三角锥;(2)SiF4⌘
点击查看答案
已知下列分子的几何构型,试用杂化轨道理论分析它们的成键情况:
(1)PCI5三角锥;(2)SiF4正四面体
(3)BF3正三角形;(4)AsI5三角双锥。
第4题
试用价层电子对互斥理论判断下列3种氟化物的分子构型,并用杂化轨道理论分析它们的成键情况。(1)BF3; (2)NF3; (3)ClF3;
试用价层电子对互斥理论判断下列3种氟化物的分子构型,并用杂化轨道理论分析它们的成键情况。(1)BF3; (2)NF3; (3)ClF3;
点击查看答案
第7题
试根据下列结构信息,用杂化轨道理论分析各分子的成键情况: (1)H2S为“V”字形结构,H-S-H键
试根据下列结构信息,用杂化轨道理论分析各分子的成键情况: (1)H2S为“V”字形结构,H-S-H键
点击查看答案
试根据下列结构信息,用杂化轨道理论分析各分子的成键情况:
(1)H2S为“V”字形结构,H-S-H键角为92°7';
(2)CS2为直线形结构,C原子与两个S原子之间均有双键;
(3)二甲醚(H3COCH3)分子为“V”字形结构,C-O-C键角约为112°;
(4)丙酮(CH3COCH3)的3个C原子和O原子共平面,O-C-C键角和C-C-C键角均接近120°,且碳氧之间存在双键。
第9题
C—H键中氢原子1s轨道与碳原子2s轨道之间的重叠积分为0.57,若取C—H为z轴,氢原子的1s轨道与碳原子
的2Pz之间重叠积分为0.467,氢原子的1s轨道和碳的指向z轴的sp、sp2、sp3杂化轨道之间的重叠积分是多少?
点击查看答案
第11题
根据下列配离子的空间构型,画出它们形成时中心离子的价层电子分布,并指出它们以何种杂化轨道成
键,估计其磁矩各为多少(BM.)?
点击查看答案
(1)/[CuCl2/]-(直线形);
(2)/[Zn(NH3)4/]2+(四面体形);
(3)/[Co(NCS)4/]2-(四面体形).


 如果结果不匹配,请
如果结果不匹配,请 

















