 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
CO2分子中,C原子的轨道杂化类型及CO2分子的空间构型是:()。
A.sp2杂化、V字型
B.sp杂化、直线型
C.sp3杂化、空间正四面体型
D.sp3杂化、三角锥型
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.sp2杂化、V字型
B.sp杂化、直线型
C.sp3杂化、空间正四面体型
D.sp3杂化、三角锥型
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“CO2分子中,C原子的轨道杂化类型及CO2分子的空间构型是:…”相关的问题
更多“CO2分子中,C原子的轨道杂化类型及CO2分子的空间构型是:…”相关的问题
A.N2分子包含一个s键和两个π键
B.CO分子中存在配位键
C.原子形成共价键时必须遵守饱和性和方向性原则
D.sp2杂化轨道是由1s和2p轨道杂化而成
A.原子轨道的杂化,只有在形成分子的过程中才会发生,而孤立的原子是不可能发生杂化的
B.只有能量相近的原子轨道才能发生杂化
C.一定数目的原子轨道杂化后,可以得到更多数量的杂化轨道
D.CH4分子中有四个能量相等的C—H键,键角为109°28′,分子的空间构型为正四面体,这一情况可以用杂化轨道理论解释
已知[Co(NH3)6]3+的μ=0,则C03+杂化轨道的类型是(9) ,配离子的空间构型是 (10) 。
试根据下列结构信息,用杂化轨道理论分析各分子的成键情况:
(1)H2S为“V”字形结构,H-S-H键角为92°7';
(2)CS2为直线形结构,C原子与两个S原子之间均有双键;
(3)二甲醚(H3COCH3)分子为“V”字形结构,C-O-C键角约为112°;
(4)丙酮(CH3COCH3)的3个C原子和O原子共平面,O-C-C键角和C-C-C键角均接近120°,且碳氧之间存在双键。
当∮αi代表α原子的i原子轨道时,∮=
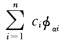 是()。
是()。
A.LCAO-MO
B.杂化轨道
C.原子的波函数
试用VSEPR理论预测下列分子或离子的几何构型,并用杂化轨道理论加以说明:
①BeCl2;②SnCl2;③NCl3;④XeF4;⑤SF6;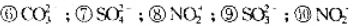
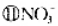 .
.