 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298.15K时,已知AgCl在纯水中的溶解度1.33×10-5·mol·L-1,计算AgCl-1的溶度积。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298.15K时,已知AgCl在纯水中的溶解度1.33×10…”相关的问题
更多“298.15K时,已知AgCl在纯水中的溶解度1.33×10…”相关的问题
A.大
B.小
C.相等
D.2倍
已知可逆反应: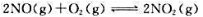 在298.15K下进时的
在298.15K下进时的 计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中
计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中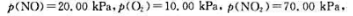 判断反应进行方向。
判断反应进行方向。
已知下列可逆反应: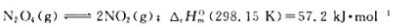 利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
298.15K时,Mg(OH)2的标准溶度积常数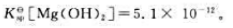 试计算:
试计算:
(1)Mg(OH)2在水中的溶解度:
(2)Mg(OH)2饱和溶液中的Mg2+、OH-的浓度和溶液的pH;
(3)Mg(OH)2在0.010mol·L-1NaOH溶液中的溶解度;
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度。
298.15K,1x10-3m3容器中的压力值,并与用理想气体状态方程计算的压力值进行比较.
已知25°C时AgCl(s).水溶液中Ag+,CI-的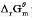 分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。
分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。
A.4.24×10-10mol/L
B.4.24×10-5mol/L
C.4.24×10-10mol/L
D.1.34×10-5mol/L
A.193kJ·mol-1
B.873kJ·mol-1
C.-193kJ·mol-1
D.-873kJ·mol-1
A.-195kJ·mol-1
B.195kJ·mol-1
C.-875kJ·mol-1
D.875kJ·mol-1