 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时,乙烷的第二、第三维里系数分别为B=-186X10-6m3·mol-1和C=1.0
298.15K,1x10-3m3容器中的压力值,并与用理想气体状态方程计算的压力值进行比较.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298.15K,1x10-3m3容器中的压力值,并与用理想气体状态方程计算的压力值进行比较.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知298.15K时,乙烷的第二、第三维里系数分别为B=-1…”相关的问题
更多“已知298.15K时,乙烷的第二、第三维里系数分别为B=-1…”相关的问题
已知可逆反应: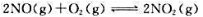 在298.15K下进时的
在298.15K下进时的 计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中
计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中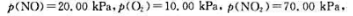 判断反应进行方向。
判断反应进行方向。
已知下列可逆反应: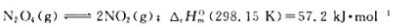 利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
A.-195kJ·mol-1
B.195kJ·mol-1
C.-875kJ·mol-1
D.875kJ·mol-1
A.193kJ·mol-1
B.873kJ·mol-1
C.-193kJ·mol-1
D.-873kJ·mol-1
KCl(s)298.15K时的溶解过程: KCl(s)==K+(aq,ao)+Cl-(aq,∞)△Hm=17.1810/mol已知Cl-(aq,∞)和KCl(s)的摩尔生成焓分别为一167.4410/mol和一435.87kJ/mol,求K+(aq,∞)的摩尔生成焓。
乙烷裂解生成乙烯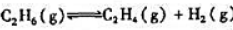 已知在1273K,100.0kPa下,反应达到平衡时,p(C2H6)=2.62kPa,p(C2H4)=48.7kPa,p(H2)=48.7kPa.计算该反应的标准平衡常数Kθ.在实际生产中可在定温定压下采用加入过量水蒸气的方法来提高乙烯的产率(水蒸气作为惰性气体加入),试以平衡移动的原理加以说明.
已知在1273K,100.0kPa下,反应达到平衡时,p(C2H6)=2.62kPa,p(C2H4)=48.7kPa,p(H2)=48.7kPa.计算该反应的标准平衡常数Kθ.在实际生产中可在定温定压下采用加入过量水蒸气的方法来提高乙烯的产率(水蒸气作为惰性气体加入),试以平衡移动的原理加以说明.
25℃和101.33kPa时乙烷(E)在正庚醇(H)中的溶解度是xE=0.0159,且液相的活度系数可以表示为lnγE=B(1一xE2),并已知25℃时的Henry常数:HE,H=27.0(在p=101.32kPa时);HE,H=162(在p=2026.4kPa时)。计算25℃、2026.4kPa时乙烷在正庚醇中的溶解度(可以认为正庚醇为不挥发组分)。
A.第一关键字
B.第二关键字
C.第三关键字
D.主要关键字
A.前方站
B.前方第一闭塞分区
C.前方第二闭塞分区
D.前方第三闭塞分区
#include<stdio.h>
main()
{float x,amax,amin;
scanf("%f",&x);
amax=x:
amin=x;
while()/*第一空*/
{if(______)amax=x;/*第二空*/
if(x<amin)______;/*第三空*/
scanf("%f",&x);
}
printf("amax=%3.2f,amin=%3.2f\n",amax,amin);
}