 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下对合成氨反应速率测得如下数据:Ac(NH3)/△t=2.0×10-4mol.L-1.s-1;如果以-△c(N2)/△t表示反
某温度下对合成氨反应速率测得如下数据:Ac(NH3)/△t=2.0×10-4mol.L-1.s-1;如果以-△c(N2)/△t表示反应速率,其值为________________mol.L-1.s-1;若以一△c(H2)/t表示反应速率,则为________________mol.L-1.s-1。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“某温度下对合成氨反应速率测得如下数据:Ac(NH3)/△t=…”相关的问题
更多“某温度下对合成氨反应速率测得如下数据:Ac(NH3)/△t=…”相关的问题
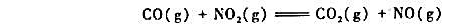
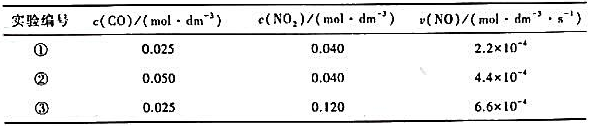
 ,求在平均温度下的反应速率与管中心处的反应速率之比。
,求在平均温度下的反应速率与管中心处的反应速率之比。

















