 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知NO(g)和NO2(g)的分别为90.3kJ·mol-1和33.2kJ·mol-1,反应NO2(g)→NO(g)+1/2O2(g)的为()。 (A) 33.2kJ·m
已知NO(g)和NO2(g)的

(A) 33.2kJ·mol-1(B) 57.1kJ·mol-1
(C) 123.5kJ·mol-1(D) 90.3kJ·mol-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知NO(g)和NO2(g)的

(A) 33.2kJ·mol-1(B) 57.1kJ·mol-1
(C) 123.5kJ·mol-1(D) 90.3kJ·mol-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知NO(g)和NO2(g)的分别为90.3kJ·mol-1…”相关的问题
更多“已知NO(g)和NO2(g)的分别为90.3kJ·mol-1…”相关的问题
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g),已知在540~727K之间发生定容反应,其速率常数k的表达式为
kc/(mol-1·dm3·s-1)=1.2×1010exp[-132kJ·mol-1/(RT)]
若在600K时,CO(g)和NO2(g)的初始压力分别为667Pa和933Pa。试计算:
A.114.8 kJ
B.232 kJ
C.368.8 kJ
D.173.4 kJ
有基元反应Cl(g)+H2(g)→HCl(g)+H(g),已知它们的摩尔质量和直径分别为
MCl=35.45g·mol-1,-1=2.016g·mol-1
dCl=0.20nm,
已知CH3COOH(g),CH4(g)和CO2(g)的平均摩尔定压热容 分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1。试由附录(在教材中)中各化合物的标准摩尔生成焓计算1000K时下列反应的
分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1。试由附录(在教材中)中各化合物的标准摩尔生成焓计算1000K时下列反应的 。
。
CH3COOH(g)===CH4(g)+CO2(g)
已知在温度为298.15K的标准条件下,CO(g)和H2O(g)的标准摩尔生成焓分别为-110.53kJ/mol和-241.83kJ/mol。计算反应H2O(g)+C(石墨)====CO(g)+H2(g)的标准摩尔焓变。
A.9.0L
B.13.5L
C.15.7L
D.16.8L
已知298.15K时,CO(g)和CH3OH(g)标准摩尔生成焓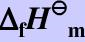 分别为-110.525和-200.66kJ/mol。CO(g)、H2(g)、CH3OH(l)的标准摩尔熵
分别为-110.525和-200.66kJ/mol。CO(g)、H2(g)、CH3OH(l)的标准摩尔熵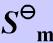 (298.15K)分别为197.67J/(mol·K)、130.68J/(mol·K)及127J/(mol·K)。又知298.15K时甲醇的饱和蒸气压16.59kPa,摩尔气化热
(298.15K)分别为197.67J/(mol·K)、130.68J/(mol·K)及127J/(mol·K)。又知298.15K时甲醇的饱和蒸气压16.59kPa,摩尔气化热 =38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应
=38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应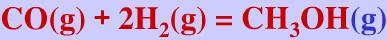 的
的
已知298.15K,CO(g)和CH3OH(g)标准摩尔生成焓△fHmΘ分别为一110.525kJ/mol和-200.67kJ/mol;CO(g)、H2(g)、CH3OH(1)的标准摩尔熵SmΘ分别为197.674,130.684及126.8J/(mol.K)。又知298.15K甲醇的饱和蒸气压为16.59kPa,摩尔气化热△HmΘ=38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应CO(g)+2H2(g)==CH3OH(g)的△rGmΘ及KpΘ。
工业上以氨气为原料制备硝酸的过程如下: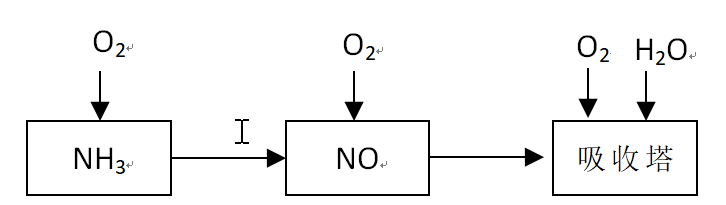 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。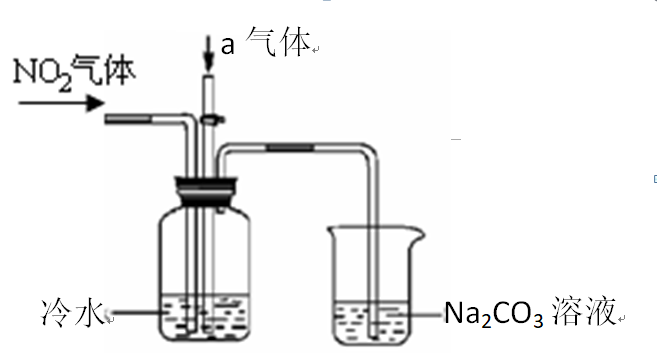
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。