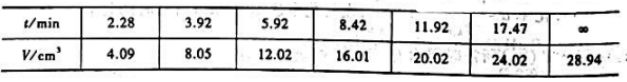
题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g),已知在540~727K之间发生定容反应,其速率常数k的表达式为 kc/(mol-
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g),已知在540~727K之间发生定容反应,其速率常数k的表达式为
kc/(mol-1·dm3·s-1)=1.2×1010exp[-132kJ·mol-1/(RT)]
若在600K时,CO(g)和NO2(g)的初始压力分别为667Pa和933Pa。试计算:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g…”相关的问题
更多“有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g…”相关的问题
 分别为90.3kJ·mol-1和33.2kJ·mol-1,反应NO2(g)→NO(g)+1/2O2(g)的
分别为90.3kJ·mol-1和33.2kJ·mol-1,反应NO2(g)→NO(g)+1/2O2(g)的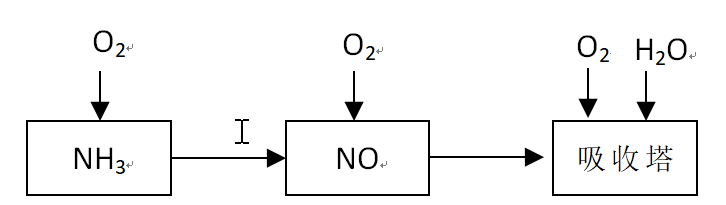 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。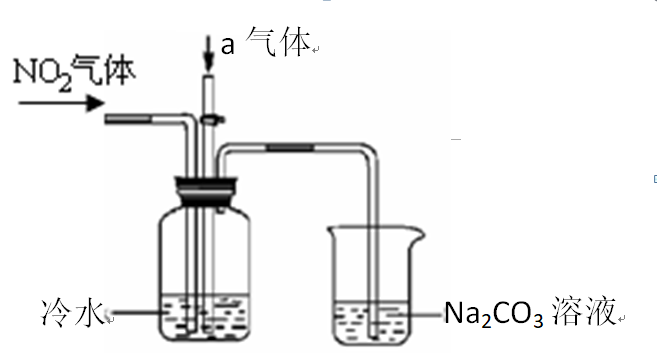
 N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。