 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应在某温度时速率系数为2.31×10-3s-1,计算: (1)反应进行了10min后,N2O
反应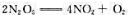 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应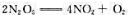 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应在某温度时速率系数为2.31×10-3s-1,计算: (…”相关的问题
更多“反应在某温度时速率系数为2.31×10-3s-1,计算: (…”相关的问题
某温度下对合成氨反应速率测得如下数据:Ac(NH3)/△t=2.0×10-4mol.L-1.s-1;如果以-△c(N2)/△t表示反应速率,其值为________________mol.L-1.s-1;若以一△c(H2)/t表示反应速率,则为________________mol.L-1.s-1。
A.正反应的活化能与逆反应的活化能相等
B.正反应的活化能大于逆反应的活化能
C.逆反应的活化能大于正反应的活化能
D.无法比较正、逆反应的活化能的相对大小
平衡常数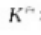 将(),反应的标准摩尔吉布斯自由能变将()。
将(),反应的标准摩尔吉布斯自由能变将()。
已知反应 在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
某温度时,反应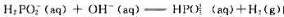 的反应速率与反应物浓度的关系如下表所示:
的反应速率与反应物浓度的关系如下表所示:

该反应的速率方程是()。
A、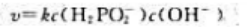
B、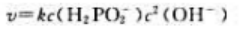
C、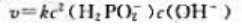
D、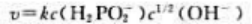
在一定温度下,反应物A(g)进行恒容反应,速率系数kA=2.0×10-3mol-1.dm.s-1,A(g)的初始浓度cA,D=0.05mol.dm-3。此反应的级数n=________,反应物A(g)的半衰期t1/2=______________。
A.1和-119.7kJ·mol-1
B.1和119.7kJ·mol-1
C.2和-119.7kJ·mol-1
D.2和119.7kJ·mol-1