 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
取100.0mL水样,在pH为10时以铬黑T为指小剂用0.01000mol·L-1EDTA标准溶液进行滴定,消耗
23.00mL.另取10.00ml.水样,调节pH为13.使Mg生成Mg(OH)2沉淀,以紫脉酸胺为指示剂.用同EDTA柯准溶液滴定,消耗10.00mL.分别计算此水样中Ca2+和Mg2+的浓度.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“取100.0mL水样,在pH为10时以铬黑T为指小剂用0.0…”相关的问题
更多“取100.0mL水样,在pH为10时以铬黑T为指小剂用0.0…”相关的问题
Na2Cr207+H2S04溶液在使用后6价铬被还原为3价铬,把此废液电解,使3价铬被氧化为6价铬。现有含260g·L-1Cr2(SO4)3+20g·L-1Na2Cr207+250g·L-1H2SO4废液,用电解法再生到90%的铬以6价态存在为止。设两电极的电流效率为l00%,电解过程中硫酸浓度变化很小。试分别计算电解开始和终止时所需槽电压的理论值,并计算再生液的最终组成。在计算中可用浓度代替活度。
设S的ω弧三角的面积函数A(θ)在θ=ξ处取绝对极大值(最大值),且K=A(ξ)/A,其中A为S的总面积.今有n个点无目的地散播于S内,以p(n)表那群点恰好落入随意一个ω弧三角内的概率,则当n→∞便有渐近式:

在浓度分别为0.020mol.L-1Cr2+和0.030mol.L-1Pb2+的混合液中,如何控制酸度(用pH表示)以氢氧化物的沉淀形式加以分离
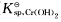 =1.2×10-15;
=1.2×10-15;
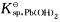 =2.6×10-31]?
=2.6×10-31]?
下列氨基酸在pH=4.0的溶液中,以负离子形式存在的是
A.谷氨酸 B.甘氨酸 C.丙氨酸 D.赖氨酸
A.1.09g/mL
B.1.0193g/mL
C.1.02g/mL
D.1.0g/mL
A.5倍
B.10倍
C.20倍
D.30~40倍