 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206kJ/molCH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247kJ/molC—H键的键能约为413kJ/mol,O—H键的键能约为463kJ/mol,H—H键的键能约为436kJ/mol,则CO2中C=O键的键能约为()。
A.797.5kJ/mol
B.900.5kJ/mol
C.962.5kJ/mol
D.1595kJ/mol
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.797.5kJ/mol
B.900.5kJ/mol
C.962.5kJ/mol
D.1595kJ/mol
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知CH4(g)+H2O(g)=CO(g)+3H2(g)△H…”相关的问题
更多“已知CH4(g)+H2O(g)=CO(g)+3H2(g)△H…”相关的问题
A.114.8 kJ
B.232 kJ
C.368.8 kJ
D.173.4 kJ
在天然气产地,可以用甲烷分解法制备H2。实际生产时是将H2O(g)和O2 (g)同时通入高温反应塔,CH4分别和它们起反应。写出这两个化学反应方程式,分别计算
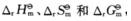 ,并说明通入O2的目的?
,并说明通入O2的目的?
A.(1)(2)
B.(1)(4)
C.(2)(3)
D.(3)(4)
煤和由煤与水蒸气反应[C(s)+H2O(g)=H2(g)+CO(g)]而得的水煤气(CO与H2等物质的混合物)都可用做燃料。设煤含碳80%,其余可燃成分忽略不计。试通过计算说明,在实际应用中以水煤气代替煤作燃料的优点。(提示:在任何能量转换过程中,总会有一些能量变成热而扩散到环境中。例如,欲往某体系输入xkJ的能量,实际上提供的热量要远多于该值。)
A.向右进行
B.向左进行
C.处于平衡状态
D.无法判断
只用下表数据:
物质 | Delta_{r}H_{m}^{Theta }/(kJcdot mol^{-1}) | Delta_{r}G_{m}^{Theta }/(kJcdot mol^{-1}) | S_{m}^{Theta }/(Jcdot mol^{-1}cdot K^{-1}) |
CO(g) | -110.5 | -137.3 | 197.9 |
CO2(g) | -393.5 | -394.4 | 213.6 |
H2O(g) | -241.8 | -228.6 | — |
H2(g) | — | — | 130.6 |
(1)计算反应的
。
(2)求H2O(g)的标准熵。
根据298.15K,pΘ时物质的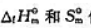 值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的
值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的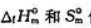 ;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
A.Q1+Q2+Q3
B.0.5Q1-0.5Q2+1.5Q3
C.0.5(Q1+Q2+Q3)
D.0.5Q1-1.5Q2+0.5Q3