 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在101.325kPa、273.15K下,1mol固体冰融化为水时的Q()0;W()0;△U()0(填>、<或=)。
在101.325kPa、273.15K下,1mol固体冰融化为水时的Q( )0;W( )0;△U( )0(填>、<或=)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在101.325kPa、273.15K下,1mol固体冰融化为水时的Q( )0;W( )0;△U( )0(填>、<或=)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在101.325kPa、273.15K下,1mol固体冰融化…”相关的问题
更多“在101.325kPa、273.15K下,1mol固体冰融化…”相关的问题
将1mol的SO2与1molO2的混合气体,在101.325kPa及903K下通过盛有铂丝的玻璃管,控制气流速度,使反应达到平衡,把产生的气体急剧冷却,并用KOH吸收SO2及SO3。最后量得余下的氧气在101.325kPa,273.15K下体积为13.78dm3,试计算反应SO2+(1/2)O2===SO3在903K时的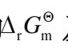 及KΘ。
及KΘ。
已知冰和水的密度分别为0.92×103kg/m3和1.0×103kg/m3,现有1 mol的水发生如下变化: (1)在373.15K、101.325kPa下蒸发为水蒸气,且水蒸气可视为理想气体; (2)在273.15K、101.325kPa下变为冰。 试求上述过程系统所作的体积功。
在101.325kPa下,1kg水中溶有不挥发的0.2molB和0.3molC物质形成稀溶液,已知水(M=18.02g/mol)的沸点升高常数kb=0.52K·kg/mol。
在100℃和101.325kPa下,1mol水等温蒸发为水蒸气(假设水蒸气为理想气体)。因为此过程中系统的温度不变,所以△U=0,Qp=∫CpdT=0。这一结论是否正确?为什么?
甲醇(CH3OH)在101.325kPa下的沸点(正常沸点)为64.65℃,在此条件下的摩尔蒸发焓△vapHm=35.32kJ·mol-1。求在上述温度、压力条件下,1kg液态甲醇全部成为甲醇蒸气时的Q,W,△U,△H及△S。
甲醇(CH3OH)在101.325kPa下的沸点(正常沸点)为64.65℃,在此条件下的摩尔蒸发焓△vapHm=35.32kJ·mol-1。求在上述温度、压力条件下,1kg液态甲醇全部成为甲醇蒸气时的Q,W,△U,△H及△S。
PCI5的分解反应为: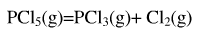 。在523.2K,101.325kPa下反应达到平衡后,测得平衡混合物的密度为2.695×103kg·m-3,试计算:
。在523.2K,101.325kPa下反应达到平衡后,测得平衡混合物的密度为2.695×103kg·m-3,试计算:
(1) PCI5(g)的解离度;(2) 该反应的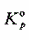 ;(3)该反应的
;(3)该反应的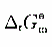 。
。