 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在101.325kPa下,1kg水中溶有不挥发的0.2molB和0.3molC物质形成稀溶液,已知水(M=18.02g/mol)的沸点升高常数k
在101.325kPa下,1kg水中溶有不挥发的0.2molB和0.3molC物质形成稀溶液,已知水(M=18.02g/mol)的沸点升高常数kb=0.52K·kg/mol。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在101.325kPa下,1kg水中溶有不挥发的0.2molB和0.3molC物质形成稀溶液,已知水(M=18.02g/mol)的沸点升高常数kb=0.52K·kg/mol。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在101.325kPa下,1kg水中溶有不挥发的0.2mol…”相关的问题
更多“在101.325kPa下,1kg水中溶有不挥发的0.2mol…”相关的问题
水中可溶解1.0g.如果用只能承受202.65kPa的瓶子充装溶有CO2(g)的饮料,则在20℃条件下充装时,CO2的最大压力为多少才能保证此瓶装饮料可以在40℃条件下安全存放?设CO2溶质服从亨利定律.
已知水(H2O,1)在100℃的饱和蒸气压P*=101.325kPa,在此温度、压力下水的摩尔蒸发焓△vapHm=40.668kJ·mol-1。求在100℃,101.325kPa下,使1kg水蒸气全部凝结成液体水的Q,W,△U,△H。设水蒸气适用于理想气体状态方程式。
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓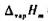 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
已知0℃,101.325kPa时,O2在水中的溶解度为4.49cm3/100g;N2在水中的溶解度为2.35cm3/100g。试计算被101.325kPa,体积分数ψ(N2)=79%,ψ(O2)=21%的空气所饱和了的水的凝固点较纯水的降低了多少?
A.压强减小,气体溶解度增大
B.压强减小,气体溶解度减小
C.温度降低,气体溶解度减小
D.气体溶解度与温度无关
在101.325kPa下,将9.0kg的水(A)与30.0kg的醋酸(B)形成的液态混合物加热到378K,达到气液两相平衡时,气相组成yB=0.417,液相中xB=0.544。求气液两相的质量各为多少kg?