 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知有A溶液浓度为14.65%NaCl溶液,又有B溶液浓度为0.75%的NaCl稀溶液,而工作需要浓度为3.50%,问利用上述二种溶液配制5000ml,浓度为3.50的工作溶液时各需AB多少ml?(用交叉法计算)。
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知有A溶液浓度为14.65%NaCl溶液,又有B溶液浓度为…”相关的问题
更多“已知有A溶液浓度为14.65%NaCl溶液,又有B溶液浓度为…”相关的问题
A、体积质量百分浓度;
B、质量百分浓度;
电池: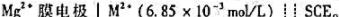 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。
(1)当用未知溶液代替上述已知Mg2+溶液时。测得电池电动势为0.425V,求此溶液的pMg为多大?
(2)若溶液替代引起液接电位Ej的不稳定值为±1mV,则Mg2+浓度测定产生的相对误差有多大?波动范围为多少?
NH4Cl和NH3·H2O的混合溶液,其pH=9.5,已知NH3·H2O的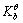 =
=
1.8×10-5。若溶液中c(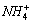 )为5.0mol·dm-3,试求溶液的c(NH3·H2O)。
)为5.0mol·dm-3,试求溶液的c(NH3·H2O)。
有一a和b两化合物混合溶液,已知a在波长282nm和238nm处的吸光系数值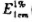 分别为720和270;而b在上述两波长处吸光度相等。现把a和b混合液盛于1.0cm吸收池中,测得λmax282nm处的吸光度为0.442;在λmax238nm处的吸光度为0.278,求a化合物的浓度(mg/100ml)。
分别为720和270;而b在上述两波长处吸光度相等。现把a和b混合液盛于1.0cm吸收池中,测得λmax282nm处的吸光度为0.442;在λmax238nm处的吸光度为0.278,求a化合物的浓度(mg/100ml)。
已知磷酸的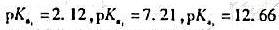 ,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序,溶液中的2种主要存在型体为()和()。
,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序,溶液中的2种主要存在型体为()和()。
某溶液中的Zn2+,Cd2+,Pb2+,Cu2+先经电积富集,后进行阳极溶出,所得的微分脉冲阳极溶出曲线如图所示,又从工作曲线获知1.0μmol·L-1的Pb2+相应的电流为12.5μA,试计算上述各离子的浓度。

习题11.7图