 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,用Ag|AgCl为电极,电解KCl的水溶液,通电前溶液中KCl的质量分数为ω(KCl)=1.4941×10-3,通电后在质量
在298K时,用Ag|AgCl为电极,电解KCl的水溶液,通电前溶液中KCl的质量分数为ω(KCl)=1.4941×10-3,通电后在质量为120.99g的阴极部溶液中ω(KCl)=1.9404×10-3,串联在电路中的银库仑计中有160.24mg的Ag沉积出来,求K+和Cl-的迁移数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在298K时,用Ag|AgCl为电极,电解KCl的水溶液,通…”相关的问题
更多“在298K时,用Ag|AgCl为电极,电解KCl的水溶液,通…”相关的问题

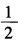 Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数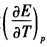 。
。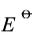 。已知298K时水的离子积Kw=1×10-14。
。已知298K时水的离子积Kw=1×10-14。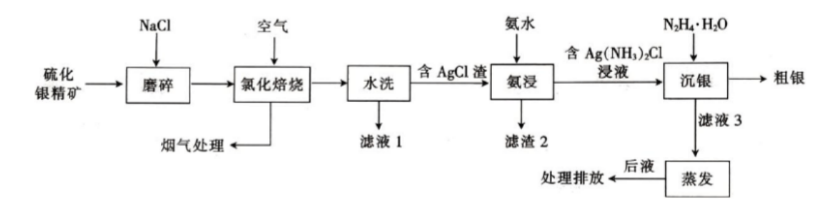 已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。
已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。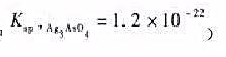 )
)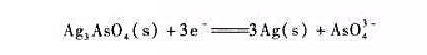
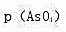 的表达式(不考虑液接电位)。
的表达式(不考虑液接电位)。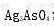 溶液中
溶液中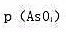 (温度为25℃)。
(温度为25℃)。
















