 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用惰性电极电解物质的量浓度相同、体积比为3∶1的硫酸铜和氯化钠的混合溶液,不可能发生的反应有()
A.2Cu2++2H2O=====电解2Cu+4H++O2↑
B.u2++2Cl-=====电解Cu+Cl2↑
C.2Cl-+2H2O=====电解2OH-+H2↑+Cl2↑
D.2H2O=====电解2H2↑+O2↑
 答案
答案
C、2Cl-+2H2O=====电解2OH-+H2↑+Cl2↑
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.2Cu2++2H2O=====电解2Cu+4H++O2↑
B.u2++2Cl-=====电解Cu+Cl2↑
C.2Cl-+2H2O=====电解2OH-+H2↑+Cl2↑
D.2H2O=====电解2H2↑+O2↑
 答案
答案
C、2Cl-+2H2O=====电解2OH-+H2↑+Cl2↑
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用惰性电极电解物质的量浓度相同、体积比为3∶1的硫酸铜和氯化…”相关的问题
更多“用惰性电极电解物质的量浓度相同、体积比为3∶1的硫酸铜和氯化…”相关的问题
A.uCl2(CuCl2)
B.NaOH(NaOH)
C.NaCl(HCl)
D.uSO4(CuO)
A.物质的量相等
B.质量相等
C.所失去的电子数相等
D.质量比为24/27/56
A.FeCl3溶液可用于铜质印刷线路板的制作,该反应是置换反应
B.用惰性电极电解含有H218O的普通水时,阳极可能产生两种相对分子质量不同的氧分子
C.反应A(g)B(g)△H,若正反应的活化能为EakJ/mol,逆反应的活化能为EbkJ/mol,则△H=-Ea-Eb)kJ/mol
D.3x%的A物质的溶液与x%的A物质的溶液等体积混合后,溶液的质量分数小于2x%,则A物质可能为乙醇
现有M、N两种气态化合物,其摩尔质量之比为2∶1,试回答下列问题:①同温同压下,M、N气体的密度之比为()。②相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度等,则两个容器中的压强之比为()。③将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为()。
芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。用如图所示装置电解硫酸钠溶液,模拟工业上离子交换膜法制烧碱的方法。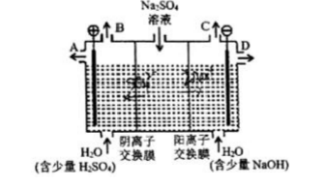 (1)该电解槽的阴极反应式为()。
(1)该电解槽的阴极反应式为()。
(2)电解时,通过阴离子交换膜的离子数()通过阳离子交换膜的离子数。(填大于、小于或等于)。
(3)制得的氢氧化钠溶液从出口()(填写“A”、“B”、“C”、“D”)导出。
(4)①若将制得的氧气、氢氧化钠溶液与天然气组合为甲烷燃料电池,则电池负极的电极反应式为()。
②若将该电池连接两惰性电极,用于电解800mLlmol/L的AgNO3溶液,当原电池中消耗CH4的体积在标况下为0.224L时,电解池中阴极将得到()g的单质,电解池中H+的浓度为()(假设溶液体积不变)。
利用如图所示装置可制取H2,两个电极均为惰性电极,c为阴离子交换膜。下列叙述正确的是()。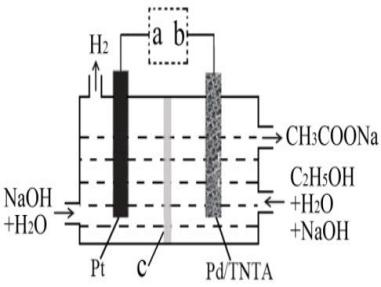
A.a为电源的正极
B.工作时,OH-向左室迁移
C.右室电极反应为:C2H5OH+H2O-4e-=CH3COO-+5H+
D.生成H2和CH3COONa的物质的量之比为2:1
A.1︰1︰1
B.1︰2︰3
C.6︰3︰2
D.3︰2︰1
A.0.5mol·L-1
B.0.8mol·L-1
C.1.0mol·L-1
D.1.5mol·L-1
A.原混合溶液中钾离子浓度为2mol/L
B.上述电解过程中共转移6mol电子
C.电解得到的铜的物质的量为0.5mol
D.电解后溶液中氢离子浓度为2mol/L