 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
胆矾是一种蓝色晶体,化学式是CuSO4•5H2O,胆矾受热时易失去结晶水,成为白色的无水CuSO4粉末,无水CuSO4易吸收水份又变成蓝色,在工业上精炼铜、镀铜等都要用胆矾.上述对胆矾的描述中,没有涉及到的是()
A.物理性质
B.用途
C.制法
D.化学性质
 答案
答案
C、制法
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.物理性质
B.用途
C.制法
D.化学性质
 答案
答案
C、制法
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“胆矾是一种蓝色晶体,化学式是CuSO4•5H2O,胆矾受热时…”相关的问题
更多“胆矾是一种蓝色晶体,化学式是CuSO4•5H2O,胆矾受热时…”相关的问题
超细纳米铜粉的比表面积大、表面活性中心数目多,在冶金和石油化工中是优良的催化剂。利用铜屑制备超细纳米铜粉的工艺流程如下: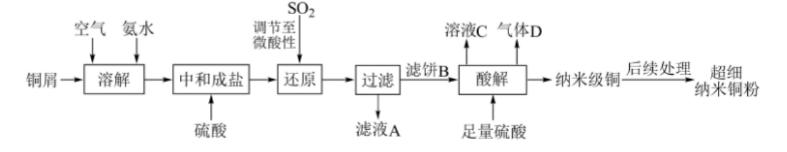 回答下列问题:
回答下列问题:
(1)“溶解”的离子方程式为(),为了加快“溶解”反应,可采取的措施有()(写出一种即可)。
(2)“滤饼B”是一种白色晶体,元素分析表明含有Cu、S、O、N、H五种元素,Cu、S、N的原子数目比为1:1:1,光谱分析显示所含阴离子呈三角锥形,其中一种阳离子呈正四面体形,则该晶体的化学式为()。
(3)“酸解”的化学方程式为();验证酸解后所得铜粉为纳米级的简便方法是()(填操作及现象)。
(4)“溶液C”可以循环利用,应将其导入到()操作中(填操作单元的名称)。
芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。用如图所示装置电解硫酸钠溶液,模拟工业上离子交换膜法制烧碱的方法。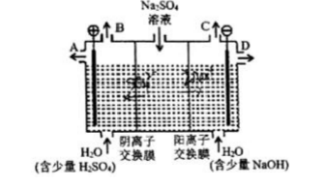 (1)该电解槽的阴极反应式为()。
(1)该电解槽的阴极反应式为()。
(2)电解时,通过阴离子交换膜的离子数()通过阳离子交换膜的离子数。(填大于、小于或等于)。
(3)制得的氢氧化钠溶液从出口()(填写“A”、“B”、“C”、“D”)导出。
(4)①若将制得的氧气、氢氧化钠溶液与天然气组合为甲烷燃料电池,则电池负极的电极反应式为()。
②若将该电池连接两惰性电极,用于电解800mLlmol/L的AgNO3溶液,当原电池中消耗CH4的体积在标况下为0.224L时,电解池中阴极将得到()g的单质,电解池中H+的浓度为()(假设溶液体积不变)。
A.向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2有酸性
B.H2S能与CuSO4溶液反应生成H2SO4,说明氢硫酸的酸性比硫酸强
C.用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,说明浓氨水呈碱性
D.常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸发应
A.原固体中一定含有K2CO3,可能含有 CuSO4和KCl
B.原固体中一定不含K2SO4和CuSO4,可能含有KCl
C.原固体中一定含有K2CO3和K2SO4,一定不含CuSO4
D.若在步骤②所得滤液中滴入AgNO3溶液,出现白色沉淀,则原固体中一定含有KCl
从含镍废催化剂中可回收镍,其流程如下: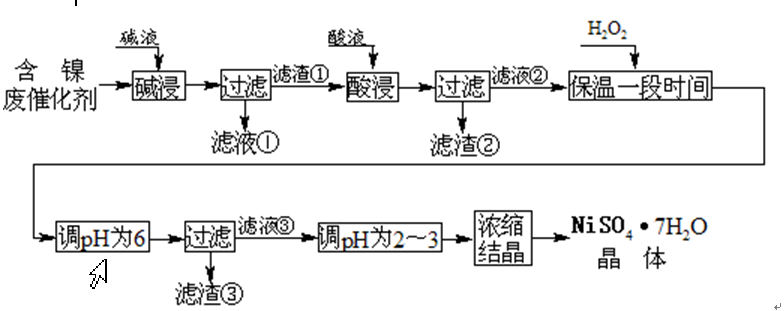 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()