 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
固体 A 的化学式为 NH5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构,与H2O反应生成H2下列说法错误的是()
A.1 molNH5 中含有 4NA个N—H 键(NA表示阿伏加德罗常数)
B.NH5中既有共价键又有离子键
C.NH5中的氢离子的电子层排布与Li+不相同
D.它与水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑
 答案
答案
C、NH5中的氢离子的电子层排布与Li+不相同
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1 molNH5 中含有 4NA个N—H 键(NA表示阿伏加德罗常数)
B.NH5中既有共价键又有离子键
C.NH5中的氢离子的电子层排布与Li+不相同
D.它与水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑
 答案
答案
C、NH5中的氢离子的电子层排布与Li+不相同
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“固体 A 的化学式为 NH5,它的所有原子的最外层都符合相应…”相关的问题
更多“固体 A 的化学式为 NH5,它的所有原子的最外层都符合相应…”相关的问题
A.NH3
B.H2O
C.N2O
D.HCl
正极材料为LiCoO2的锂离子电池被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
问题一、橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是()。
②共沉淀反应的化学方程式为()。
③高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的导电性能外,还能()。
问题二、废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过以下实验方法回收钴、锂 。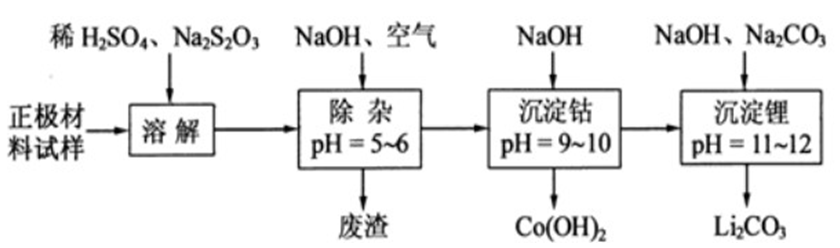
①在上述溶解过程中,S2O32ˉ被氧化成SO42ˉ,LiCoO2在溶解过程中反应的化学方程式为()。
②Co(OH)2在空气中加热时,固体残留率随温度的变化如以下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体成分为()。(填化学式);在350~400℃范围内,剩余固体成分为()。(填化学式) 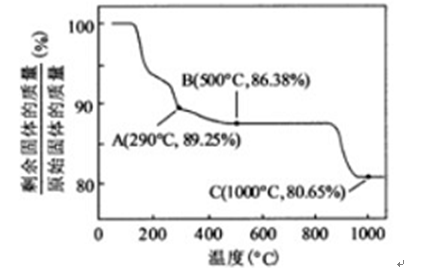
A.Y2O3
B.YO3
C.Y2O5
D.YO
A.25H50COOH
B.26H41COOH
C.25H39COOH
D.26H47COOH
A.巴基球是纯净物
B.巴基球由分子构成
C.巴基球的相对分子质量为720
D.巴基球分子由60个碳原子构成
A.次氯酸钠中氯的化合价为+1价
B.次氯酸钠属于氧化物
C.次氯酸钠中各元素的质量比为:23:35.5:16
D.次氯酸钠的相对分子质量为74
A.一个青蒿素分子由42个原子构成
B.青蒿素的相对分子质量为282
C.H、O元素的质量比为15:22:5
D.青蒿素由3种元素组成
)中滴加适量NaOH溶液得白色沉淀(D),加入过量NaOH溶液时,(D)溶解得无色溶液(E)。向(E)中加入NaClO溶液并微热,有棕黑色沉淀(F)生成。将(F)洗净后在一定温度下加热又得(A)。用硝酸处理(A)得沉淀(F)和溶液(C)。向(F)中加入盐酸有白色沉淀(G)和气体(H)生成,(H)可使淀粉碘化钾试纸变蓝。将(G)和KI溶液共热,冷却后有黄色沉淀(Ⅰ)生成。试给出(A),(B),(C),(D),(E),(F),(C),(H)和(I)所代表的物质的化学式,并写出有关化学反应方程式。
推理判断:
某盐(A)与盐酸反应,生成(B)的溶液和气体(C)。向(B)的浓溶液中加锑酸钾,析出白色晶状沉淀(D)。将气体(C)通入碘化钾溶液,生成(E)和(F),(E)使溶液发黄,(F)与过量硝酸铅生成白色沉淀(C),(G)溶于过量氢氧化钠溶液得(H),(H)与(A)反应生成黑色沉淀(I)。(I)加到硫酸锰溶液中可使溶液变成紫红色,说明有离子(J)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)的化学式,并完成各步的化学反应方程式。
(2)白色固体(A)高温下分解成(B)和气体(C)。白色固体(B)与碳在更高的温度下共热生成(D),灰黑色固体(D)与水作用生成重要工业燃气(E)和化合物(F)。(B)与稀盐酸反应生成(G)的溶液。电解(G)的无水熔盐得(H)和气体(I)。金属(H)在高温下与(J)化合成为(K),白色晶体(K)与水反应的产物中有(F)。气体(J)在(I)中燃烧的产物溶于水得盐酸。(D)在高温下与水蒸气作用,其固体产物为(A),气体产物为(C)和(J)。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I),(J)和(K)的化学式,并完成各步的化学反应方程式。