 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
坐标图中,横坐标为加入(或通入)物质的物质的量,纵坐标为生成沉淀的物质的量。下列与图示对应关系正确的是()
A.饱和石灰水中通过量CO2
B.AlCl3溶液中通过量NH3
C.MgCl2、AlCl3混合溶液中逐滴滴加NaOH溶液至过量
D.含少量HCl的AlCl3溶液中逐滴滴加NaOH溶液至过量
 答案
答案
A、饱和石灰水中通过量CO2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.饱和石灰水中通过量CO2
B.AlCl3溶液中通过量NH3
C.MgCl2、AlCl3混合溶液中逐滴滴加NaOH溶液至过量
D.含少量HCl的AlCl3溶液中逐滴滴加NaOH溶液至过量
 答案
答案
A、饱和石灰水中通过量CO2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“坐标图中,横坐标为加入(或通入)物质的物质的量,纵坐标为生成…”相关的问题
更多“坐标图中,横坐标为加入(或通入)物质的物质的量,纵坐标为生成…”相关的问题
(1)向稀硫酸中逐滴加入氢氧化钠溶液_______________;
(2)向氢氧化钠溶液中逐滴加水稀释_______________;
(3)向水中不断通入二氧化碳_______________;
(4)向水中加入熟石灰_______________。
A.氨气(水) 通入浓硫酸
B.硝酸铜(硝酸银) 加入过量铁粉,过滤
C.食盐(纯碱) 加入适量的硝酸钙溶液
D.氯化钾(硫酸钾) 加入适量的氯化钡溶液,过滤
A.碳酸钠固体(碳酸氢钠):加热法
B.碳酸氢钠溶液(碳酸钠):通入足量的二氧化碳
C.碳酸钠溶液(碳酸氢钠):加入适量的石灰水
D.碳酸钠溶液(碳酸钙):过滤法
能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO的燃烧热(△H)分别为-a()kJ•mol-1、-bkJ•mol-1、-ckJ•mol-1;②H2O(l)=H2O(g);△H=+dkJ•mol-1
则△H1=()(用含字母a、b、c、d的代数式表示)kJ•mol-1。
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)⇌CH3OH(g)△H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
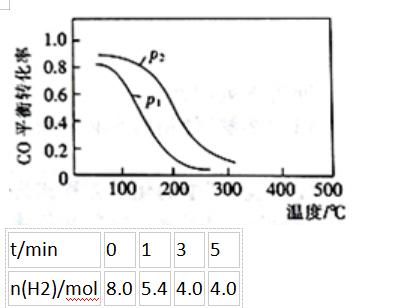 ①△H2()(填“>”“<”或“=”)0。
①△H2()(填“>”“<”或“=”)0。
②下列说法正确的是()(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③0〜3min内用CH3OH表示的反应速率v(CH3OH)=()mol•L-1·min-1。(计算结果保留两位有效数字)
④200℃时,该反应的平衡常数K=()。向上述200℃达到平衡的恒容密闭容器中再加入2molCO、2molH2、2molCH3OH,保持温度不变,则化学平衡()(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6L甲烷,测得电路中转移1.2mol电子,则甲烷的利用率为()。
A.Zn粉(Fe):用ZnCl2溶液浸泡,过滤
B.炭粉(MnO2):滴入H2O2溶液,过滤
C.NaCl溶液(Na2SO4):加入适量MgCl2溶液过滤
D.O2(H2O):通过盛有浓H2SO4的洗气瓶
A.(5,-3)或(-5,-3)
B.(-3,5)或(-3,-5)
C.(-3,5)
D.(-3,-3)
A.O2(CO) 通入O2, 点燃
B.KCl (MnO2) 加入水,充分溶解、过滤、蒸发
C.NaCl(Na2CO3) 足量加入硝酸溶液
D.u(NO3)2溶液 (AgNO3) 加入过量的铁粉,过滤
A.原白色粉末的组成有3组可能
B.原白色粉末中一定含有CaCO3
C.原白色粉末中一定不含有CuSO4
D.若向无色滤液X中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl2、NaOH
A.木炭在空气中燃烧发出白光
B.铁钉加入硫酸铜溶液后取出,铁钉表面有红色物质生成
C.二氧化碳通入石蕊试液,试液变红,加热后红色消失变为无色
D.硫在空气中燃烧发出蓝紫色火焰
A.高斯投影每带中央经线以东的Y坐标通用值均大于500km
B.1:5万地形图的带好可以在全值坐标的横坐标上看出来
C.在口述报告中,应先报目标性质,后报坐标和指示物
D.1:10万地形图上的平面直角坐标网方格边长是1cm