 更多“所有氧化还原滴定反应达到化学计量点时的电极电位与该时溶液中各…”相关的问题
更多“所有氧化还原滴定反应达到化学计量点时的电极电位与该时溶液中各…”相关的问题
第1题
用Ox1滴定Red2,氧化还原反应为:电对的电极反应及电极电位分别为:试证明化学计量点的电
用Ox1滴定Red2,氧化还原反应为:
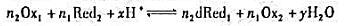
电对的电极反应及电极电位分别为:
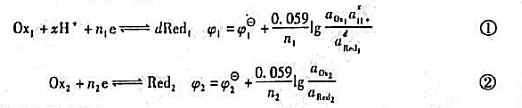
试证明化学计量点的电位为:
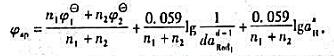
第2题
氧化还原滴定化学计量点附近的电位突跃的大小和氧化剂与还原剂两电对的( )有关,它们相差愈( ),电位突跃愈( )。
氧化还原滴定化学计量点附近的电位突跃的大小和氧化剂与还原剂两电对的()有关,它们相差愈(),电位突跃愈()。
点击查看答案
第5题
在0.10mol·L-1 HCl介质中, 用0.2000mol·L-1Fe3+滴定0.1000mol·L-1
在0.10mol·L-1HCl介质中, 用0.2000mol·L-1Fe3+滴定0.1000mol·L-1Sn2+,试计算在化学计量点时的电势及其突跃范围。在此滴定中选用什么指示剂?滴定终点与化学计量点是否一致?已知在此条件下Fe3+/Fe2+电对Eθ=0.73V,Sn4+/Sn²+,电对的Eθ=0.07v
点击查看答案
第6题
现用0.100 0 mol·L-1NaOH滴定分析浓度为0.100 0 mol·L-1的二元酸H2X。当加入NaOH25 mL时,测得溶液
的pH=4.80;当加人NaOH 50 mL时,达到第一化学计量点,溶液的pH值为7.15,试问该二元酸的Ka2值()。
点击查看答案
A.5.62×10-10
B.3.2×10-10
C.8.4×10-9
D.7.1×10-8
第10题
如以0.2000mol·L-1NaOH标准溶液滴定0.2000mol·L-1邻苯二甲酸氢钾溶液,化学计量点时的pH为多少?化学计量点附近滴定突跃为多少?应选用何种指示剂指示终点?
第11题
NaAc溶液(0.10mol/L)30ml稀释至70ml,用HCl溶液(0.10mol/L)滴定,计算化学计量点时的pH和超过计量点2滴(0.1ml)时的pH,这一滴定可行吗?


 如果结果不匹配,请
如果结果不匹配,请 

















