 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.10 mol·L-1HCl溶液滴定0.16 g纯Na2CO3(M=106 g·mol-1)至甲基橙变色为终点,约需HCl溶液()。A.1
用0.10 mol·L-1HCl溶液滴定0.16 g纯Na2CO3(M=106 g·mol-1)至甲基橙变色为终点,约需HCl溶液()。
A.10 mL
B.20 mL
C.30 mL
D.40 mL
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.10 mol·L-1HCl溶液滴定0.16 g纯Na2CO3(M=106 g·mol-1)至甲基橙变色为终点,约需HCl溶液()。
A.10 mL
B.20 mL
C.30 mL
D.40 mL
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用0.10 mol·L-1HCl溶液滴定0.16 g纯Na2…”相关的问题
更多“用0.10 mol·L-1HCl溶液滴定0.16 g纯Na2…”相关的问题
A.3个
B.2个
C.4个
D.1个
用0.100 0 mol·L-1HCl滴定同浓度的NH3溶液至化学计量点时的质子平衡方程式是()。
A.[H+]=[NH3]+[OH-]
B.[H+]+[NH4+]=[OH-]
C.[H+]=[Cl-]+[OH-]
D.[H+]+[NH4+]=[cl-]+[OH-]
用0.1000 mol·L-1NaOH标准溶液滴定0.10 mol·L-1HCI和0.10 mol·L-1H3P04混合溶液时,可能有(8) 个滴定突跃。已知:H3P04的Kθa1 =7.5×10-3,Kθa2=6.2×10-8,Kθa3=2.2×10-13。
用0.1000 mol·L-1NaOH溶液滴定0.10 mol·L-1H2C2O4溶液,应选择的指示剂为
A.溴甲酚绿 B.甲基红 C.酚酞 D.中性红
A.氢氧化钠滴定液(0.10 mol/ml)
B.0.10 mol/L氢氧化钠溶液
C.氢氧化钠滴定液(0.10 N)
D.氢氧化钠滴定液(0.10 mol/L)
用0.2000mol·L-1NaOH溶度滴定0.2000mol·L-1HCl与0.02000mol·L-1HAc混合溶液中的HCl,问:
22.用0.2000mol·L-1NaOH溶度滴定0.2000mol·L-1HCl与0.02000mol·L-1HAc混合溶液中的HCl,问:
用0.1000mol·L-1NaOH标准溶液滴定0.10mol·L-1HCl和0.10mol·L-1H3PO4混合溶液时,可能有______个滴定突跃。已知:H3PO4的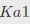 =7.5×10-3,
=7.5×10-3,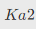 =6.2×10-8,
=6.2×10-8,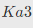 =2.2×10-13。
=2.2×10-13。
31.已知Na2CO3、NaHCO3混合溶液的pH=10.55,取其25.00mL,用0.1000mol·L-1HCl溶液滴定。当pH=6.38时,消耗HCl21.00mL。求Na2C03和NaHCO3的浓度。已知:H2CO3的 =6.38,
=6.38,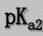 =10.25。
=10.25。