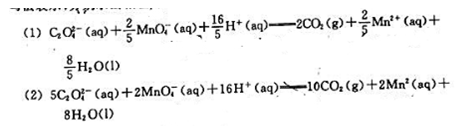题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
硝基乙酸在酸性溶液中的分解反应(NO2)CH2COOH(1)→CH3NO2(I)+CO2(g)为一级
硝基乙酸在酸性溶液中的分解反应
(NO2)CH2COOH(1)→CH3NO2(I)+CO2(g)
为一级反应.25℃,101.3kPa下,测定不同反应时间产生的CO2(g)体积如下:
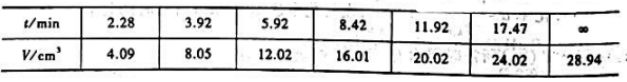
反应不是从t=0开始的.求速率常数k.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
硝基乙酸在酸性溶液中的分解反应
(NO2)CH2COOH(1)→CH3NO2(I)+CO2(g)
为一级反应.25℃,101.3kPa下,测定不同反应时间产生的CO2(g)体积如下:

反应不是从t=0开始的.求速率常数k.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“硝基乙酸在酸性溶液中的分解反应(NO2)CH2COOH(1)…”相关的问题
更多“硝基乙酸在酸性溶液中的分解反应(NO2)CH2COOH(1)…”相关的问题
高温下乙酸分解反应如下:
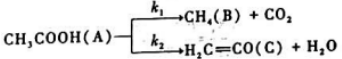
在1089K时,k1=3.74s-1,k2=4.65s-1
(1)试计算乙酸反应掉99%所需的时间;
(2)当乙酸全部分解时,在给定温度下能够获得乙烯酮的最大产量是多少?
在酸性溶液中,反应 的速率方程为v=
的速率方程为v=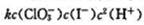 .在下列三项中,影响反应速率的因素有(),影响速率常数的因素为().
.在下列三项中,影响反应速率的因素有(),影响速率常数的因素为().
①在反应中加人水;②在反应溶液中加入氨;③反应溶液从20℃加热到35℃.
由附表六中查出酸性溶液中
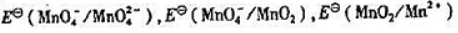
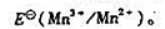
(1)颐出锰元素在酸性溶液中的元素电势图;
(2)计算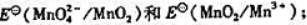
(3)MnO42-能否歧化?写出相应的反应方程式,并计算该反应的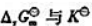 还有哪些物质能歧化?
还有哪些物质能歧化?
(4)计算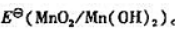
在酸性溶液中,草酸被高锰酸钾氧化的反应方程式为
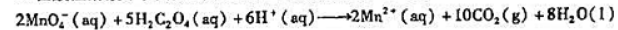
其反应速率方程为: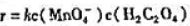 确定各反应物种的反应级数和反应的总级数.反应速率系数和单位如何?
确定各反应物种的反应级数和反应的总级数.反应速率系数和单位如何?
在水溶液中SO2作为还原剂还原(a)KMnO4溶液到MnSO4;(b)K2Cr2O7的酸性溶液到Cr3+离子;(c)Hg(NO3)2水溶液到金属汞。写出这些反应的方程式。
将Fe、Mg合金4.00g投入到足量的一定浓度的硝酸中,金属与硝酸完全反应(金属全部溶解),共收集到标准状况下的气体VL(气体为NO和NO2),若向反应后的溶液中加入足量的氢氧化钠溶液,理论上最多可得沉淀8.25g,则V值可能为()。
A.8.23
B.1.86
C.5.60
D.5.34
根据教材附表一中的相关数据主考虑电势图N2-HN4+,(aq)-NH;(aq)在酸性溶液中Eθ(N2/HN3)和Eθ(HN3/NH4+).写出HN3(aq)的岐化反应方程,计算25℃下该反应的标准平衡常数Kθ并评价NH3(aq)的稳定性.
4-)=0.08mol·dm-1的高锰酸钾溶液20cm3在100kPa和298K混合使之反应,用热量计测得的热量为-1200J。该反应的计量方程可用下面两种写法表示,分别求出相应的ξ 和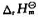 (298K) ;
(298K) ;