 更多“当活度系数固定不变时,电池电动势与被测离子浓度呈线性关系。(…”相关的问题
更多“当活度系数固定不变时,电池电动势与被测离子浓度呈线性关系。(…”相关的问题
第1题
25°C时.电池ZnIZnCl2(0.55mol.Kg-1)IAgCl(s)IAg的电动势E=1.015V.已知E(Zn2+
25°C时.电池ZnIZnCl2(0.55mol.Kg-1)IAgCl(s)IAg的电动势E=1.015V.已知E(Zn2+
点击查看答案
IZn)=-0.7620V.E-[CI-IAgCl(s)IAgI=0.2222V.电池电动势的温度系数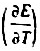 =-4.02x10-4V·K-1.
=-4.02x10-4V·K-1.
(1)写出电池反应;
(2)计算反应的标准平衡常数Kθ;
(3)计算电池反应可逆热Qr,m;
(4)求溶液中ZnCl2的平均离子活度因子ya.
第2题
称取一不纯有机一元弱酸试样2.3070g,其纯度为49.00%。将其溶于50.00ml水中,在25℃时,用0.2000mol
/L的NaOH溶液滴定。当中和一半弱酸时,用甘汞电极作正极,氢电极(Pt)H+/H2作负极,测其电动势为E1=0.58V,化学计量点时,测得电池电动势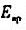 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。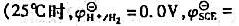
点击查看答案
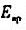 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。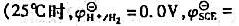
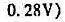
第7题
有一含NaClO3的未知溶液,取50.0ml以离子电极测定,当把1.00×10-2mol/L的NaClO3溶液加入被测试液中的体积分别
有一含NaClO3的未知溶液,取50.0ml以
第9题
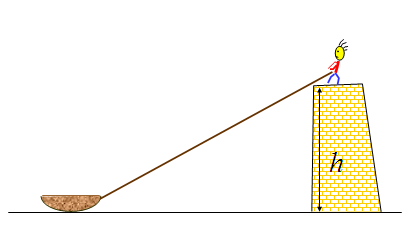
在堤岸顶上用绳子拉小船。设岸顶离水面的高度为20m,收绳子的速度为3m/s,且保持不变, 若当船与岸顶的距离为40m时开始计时,则5秒时小船速度与加速度的大小分别为 m/s和 m/s2 。
第11题
110℃时,水(1)-正丁醇(2)液液平衡数据为x'1=0.9788,x"2=0.6759。试计算汽相的组成y及总压p。 已知饱
110℃时,水(1)-正丁醇(2)液液平衡数据为x'1=0.9788,x"2=0.6759。试计算汽相的组成y及总压p。
已知饱和蒸气压为:
活度系数采用Van Laar方程计算:
其中A、B为活度系数方程参数。


 如果结果不匹配,请
如果结果不匹配,请 

















