 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
300K时,反应的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和
300K时,反应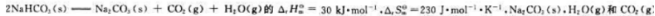 的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
300K时,反应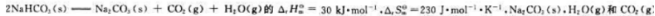 的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“300K时,反应的标准摩尔生成吉布斯自由能AGR分别为-10…”相关的问题
更多“300K时,反应的标准摩尔生成吉布斯自由能AGR分别为-10…”相关的问题
估算在400K,101.325kPa下汽相混合物的平衡组成(以摩尔分数表示),该气体含有正戊烷、异戊烷和新戊烷异构体。在400K下反应的标准生成热数据为:
5C(s)+6H2(g)====n-C5H12(g) △Gf=40.195kJ·mol-1
5C(s)+6H2(g)====i-C5H12(g) △Gf=34.415kJ·mol-1
5C(s)+6H2(g)====n-C5H12(g) △Gf=37.640kJ·mol-1
A.193kJ·mol-1
B.873kJ·mol-1
C.-193kJ·mol-1
D.-873kJ·mol-1
A.-195kJ·mol-1
B.195kJ·mol-1
C.-875kJ·mol-1
D.875kJ·mol-1
如下图所示,将一半径为r的固体球体的一半浸没在液体中,设固体和液体的表面张力分别为σg-s和σg-l固液界面张力为σs-l则在恒温、恒压下,球在浸没前后的表面吉布斯函数变化为△Gs=____________________________________________。
.jpg)
A.欧茨(Oates)的财政联邦主义理论
B.提布特(Tiebout)的“用脚投票’’理论
C.布坎南(Buchanan)的俱乐部理论
D.斯蒂格勒(Stigler)的最优分权理论
KCl(s)298.15K时的溶解过程: KCl(s)==K+(aq,ao)+Cl-(aq,∞)△Hm=17.1810/mol已知Cl-(aq,∞)和KCl(s)的摩尔生成焓分别为一167.4410/mol和一435.87kJ/mol,求K+(aq,∞)的摩尔生成焓。