 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
沉淀Al3+时,为了得到易于分离和洗涤的沉淀,应该是()
A.NH40H为沉淀剂
B.用8_羟基喹啉为沉淀剂
C.用NaOH为沉淀剂并加入NaCl电介质
D.以上三项都不对
 答案
答案
B、用8_羟基喹啉为沉淀剂
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.NH40H为沉淀剂
B.用8_羟基喹啉为沉淀剂
C.用NaOH为沉淀剂并加入NaCl电介质
D.以上三项都不对
 答案
答案
B、用8_羟基喹啉为沉淀剂
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“沉淀Al3+时,为了得到易于分离和洗涤的沉淀,应该是()”相关的问题
更多“沉淀Al3+时,为了得到易于分离和洗涤的沉淀,应该是()”相关的问题
NaOH小体积沉淀分离法常用于Al3+和Fe3+的分离。分离步骤是将试液蒸发至2~3mL后加入固体______约5g,搅拌使之呈砂粒状,再加______进行小体积沉淀。最后以适量热水稀释后过滤。
A.洗涤时离心速度过高、时间过长,白细胞等会沉淀,达不到分离的效果
B.洗涤红细胞的目的是除去血浆中的葡萄糖、无机盐
C.洗涤过程中用0.1%的生理盐水
D.透析的目的是去除样品中相对分子质量较大的杂质
A.洗涤红细胞的目的是去除血浆中的葡萄糖、无机盐
B.洗涤时离心速度过小,时间过短,白细胞等会沉淀,达不到分离的结果
C.洗涤过程选用质量分数为0.1%的NaCl溶液(生理盐水)
D.透析的目的是去除样品中相对分子质量较小的杂质
锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为MnO2,含少量FeO、A1A、Si02等杂质)为原料制备锰酸锂的流程如下图所示。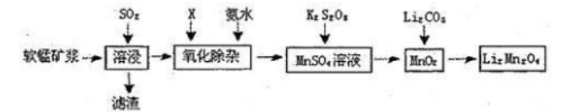 (1)溶浸生产中为提高SO2吸收率可采取的措施有()(填序号)。
(1)溶浸生产中为提高SO2吸收率可采取的措施有()(填序号)。
A、不断搅拌,使SO2和软锰矿浆充分接触
B、增大通入SO2的流速
C、减少软锰矿浆的进入量
D、减小通入SO2的流速
(2)已知:室温下,Ksp[A1(OH)3]=1×10-33,,Ksp[Fe(OH)3]=l×10-39,pH=7.1时Mn(OH)2开始沉淀。氧化除杂时(室温)除去MnSO4液中的Fe3+,Al3+(使其浓度小于1×l06mol.L-1),需调节溶液范围为()。
(3)由硫酸锰与K2S2(V溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。请写出发生反应的离子方程式()。
(4)将MnO2和Li2O3按4:1的物质的量比配料,混合搅拌,然后升温至600℃〜750℃,制取产品LiMn2O4。写出该反应的化学方程式()。
(5)锰酸锂可充电电池的总反应为:Li1-xMn2O4+LixC LiMn2O4+C(0
LiMn2O4+C(0
<x<1)
①充电时,电池的阳极反应式为(),若此时转移lmole-,则石墨电极将增重g。
②废旧锰酸锂电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是()。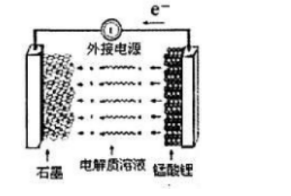
A.在FeO•FeyCrxO3中y=3x
B.反应中共转移的电子数为3xnNA(NA表示阿伏加德罗常数的值)
C.该反应中Cr2O72-是氧化剂,铁铵矾是还原剂
D.处理废水中Cr2O72-时,消耗铁铵矾的物质的量为3nxmol