 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应A2(g)+2B2(g)≒ 2AB2(g)+Q,下列说法正确的()
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
 答案
答案
B、升高温度有利于反应速率增加,从而缩短达到平衡的时间
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
 答案
答案
B、升高温度有利于反应速率增加,从而缩短达到平衡的时间
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应A2(g)+2B2(g)≒ 2AB2(g)+Q,下列…”相关的问题
更多“已知反应A2(g)+2B2(g)≒ 2AB2(g)+Q,下列…”相关的问题
气相反应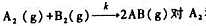 和B2均为一级.现在一个含有过量固体A2(s)
和B2均为一级.现在一个含有过量固体A2(s)
的反应器中充人50.663kPa的B2(g).已知673.2K时以反应的速率常数k=9.869x10-9kPa-1.
g-1,A,(s)的饱和蒸气压为121.59kPa[假设,A2(s)与A2(g)处于快速平衡],且没有逆反应.
(1)计算所加入的B2(g)反应掉一半所需要的时间;
(2)验证下述机理符合二级反应速率方程.

某基元反应2A(g)+B(g)=C(g)+D(g)的初始分压PA=81.04 kPa,PB=60.78 kPa。当反应至PC=20.2 kPa时,反应速率大约是初始速率的
A.1/6 8.1/16 C.1/24 D.1/48
A.0.25倍
B.4倍
C.8倍
D.相等
A.气体总质量不变
B.混合气体密度不变
C.反应物B的浓度不变
D.混合气体平均相对分子质量不再改变
已知下列两个反应:
(1)2H2(g)+O2(g)=2H2O(1);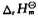 (298K)=-571.70kJ·mol-1
(298K)=-571.70kJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g);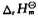 (298K)=-483.65kJ· mol-1
(298K)=-483.65kJ· mol-1
求298K时水的标准摩尔汽化热。
已知NO(g)和NO2(g)的

(A) 33.2kJ·mol-1(B) 57.1kJ·mol-1
(C) 123.5kJ·mol-1(D) 90.3kJ·mol-1
A.△H是CO2(g)的生成热
B.△H是CO(g)的燃烧热
C.△H<0
D.△H=△U
 则反应开始前p总=(),反应进行的方向是().
则反应开始前p总=(),反应进行的方向是().
已知丙烯C3H6(g)的标准摩尔燃烧热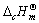 =-2058.0kJ·mol-1,试求恒容反应
=-2058.0kJ·mol-1,试求恒容反应
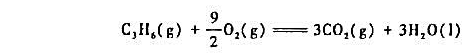
的热效应。