 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在水溶液中溴可与镁发生下列反应:Mg+Br2===MgBr2,在碱性溶液中溴能发生下列反应:3Br2+6NaOH===NaBrO3+5NaBr+3H2O。下列物质分别加入溴水中,溴水颜色不变浅的是()
A.Cl4
B.KOH晶体
C.少量HCl晶体
D.Mg
 答案
答案
C、少量HCl晶体
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Cl4
B.KOH晶体
C.少量HCl晶体
D.Mg
 答案
答案
C、少量HCl晶体
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知在水溶液中溴可与镁发生下列反应:Mg+Br2===MgB…”相关的问题
更多“已知在水溶液中溴可与镁发生下列反应:Mg+Br2===MgB…”相关的问题
简要回答下列问题:
(1)电解NaCl熔盐制取金属Na的过程中,为什么要加入CaCl2?由此带来的负面影响是什么?
(2)为什么金属Mg与冷水反应极慢,却可以迅速与热水或NH4Cl水溶液发生反应?
(3)什么是离子势φ?为什么φ的大小可以影响一些氧化物的水化物的解离方式?
(4)为什么加热MgCl2·6H2O时得不到无水盐?
(5)为降低煤炭燃烧时排向大气的SO2量,可以把CaO或CaCO3掺到含硫的煤炭中。试说明这种做法的化学原理,写出相关的化学反应方程式。
(6)Li+和Mg2+半径十分接近,试分析它们的碳酸盐分解温度的高低。
(7)锂的第一电离能比钠大,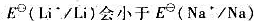 ?既然
?既然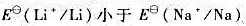 ,为什么锂与水的反应却不如钠剧烈?
,为什么锂与水的反应却不如钠剧烈?
(8)试说明锂的哪些性质与镁相似而有别于钠、钾。
(9)试说明铍的哪些性质与铝相似而有别于镁、钙。
(10)试用价层电子对互斥理论和杂化轨道理论,讨论XeF6分子的几何构型和中心原子的轨道杂化方式。
S-2-溴戊烷在氢氧化钠水溶液中水解,发生构型转化,产物的名称是 (18) ;此反应主要是按 (19) 反应历程进行的。
A.地球上99%的溴元素以溴单质形式存在于海洋中
B.在每升海水中含量低于1 mg的元素称为海水中的微量元素
C.海水是锂元素的一个重要来源
D.世界上生产的镁大部分来自海水
A.镁能从硝酸银溶液中置换出银
B.镁跟硝酸银溶液反应会生成氢气
C.根据该实验可判断镁比银化学活动性强
D.镁投入硝酸银溶液中只发生2AgNO3+Mg=Mg(NO3)2+2Ag
A.固体混合物中镁元素的质量为4.8g
B.反应后所得溶液中溶质的质量为24g
C.固体混合物中镁元素质量为2.4g
D.反应后所得溶液中溶质的质量为12g
海水开发利用的部分过程如图所示。下列有关说法不正确的是()。
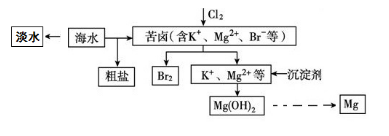
A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B.空气吹出法是工业规模海水提溴的常用方法。其工艺的其中一个环节是把氯气通入酸化的浓缩海水(或苦卤)中
C.稀有气体(如氩)氛围中和加热条件下,可以用镁与TiCl4反应得到钛
D.在工业上一般选用氢氧化钠溶液作为图示中的沉淀剂
A.被还原的元素是碳
B.镁着火,用泡沫灭火器灭火
C.的单质只存在金刚石和石墨两种同素异形体
D.该反应中化学能全部转化为热能
A.钠和镁分别与冷水反应,判断钠与镁的金属活动性强弱
B.铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断铁与钠的金属活动性强弱
C.酸性H2CO3<H2SO4,判断碳与硫的非金属活动性强弱
D.r2与I2分别与足量的H2反应的难易,判断溴与碘的非金属活动性强弱
下列物质的酸性水溶液(浓度均为1.0mol·dm-3),分别通入100kPa的氧气,能发生反应的是
已知: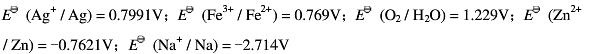 。
。
(A) AgNO3(B) ZnCl2(C) FeSO4(D) NaNO3