 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知磷酸的,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序,溶液中的2种主要存在型体为( )和( )。
已知磷酸的,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序,溶液中的2种主要存在型体为()和()。
已知磷酸的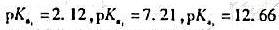 ,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序,溶液中的2种主要存在型体为()和()。
,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序,溶液中的2种主要存在型体为()和()。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知磷酸的,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序…”相关的问题
更多“已知磷酸的,若控制磷酸盐溶液的pH=6.0,则按浓度大小顺序…”相关的问题
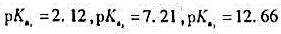 ,若控制磷酸盐溶液的pH=6.0时,溶液中两种主要存在型体为()。
,若控制磷酸盐溶液的pH=6.0时,溶液中两种主要存在型体为()。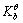 =
=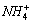 )为5.0mol·dm-3,试求溶液的c(NH3·H2O)。
)为5.0mol·dm-3,试求溶液的c(NH3·H2O)。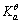 。
。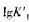 值。已知Hg2+-CN-络合物的逐级形成常数
值。已知Hg2+-CN-络合物的逐级形成常数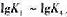 分别为:18.00,16.70,3.83和2.98.
分别为:18.00,16.70,3.83和2.98. 为2.0、5.0、7.0、10.0; M(OH)42+的
为2.0、5.0、7.0、10.0; M(OH)42+的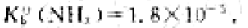 现有2.00L0.500mol·L-1NH3溶液和2.00L0.500mol·L-1HCl溶液,在25℃时,若配制pH=9.60的缓冲溶液,不允许再加水,最多能配制多少升缓冲溶液?此缓冲溶液的缓冲容量为多少?
现有2.00L0.500mol·L-1NH3溶液和2.00L0.500mol·L-1HCl溶液,在25℃时,若配制pH=9.60的缓冲溶液,不允许再加水,最多能配制多少升缓冲溶液?此缓冲溶液的缓冲容量为多少?
















