 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
下列电池Pt Sn4+,Sn2+溶液II标准甘汞电极30℃时,测得E=0.07V.计算溶液中比值(忽略
下列电池Pt Sn4+,Sn2+溶液II标准甘汞电极30℃时,测得E=0.07V.计算溶液中比值(忽略
下列电池Pt Sn4+,Sn2+溶液II标准甘汞电极30℃时,测得E=0.07V.计算溶液中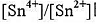 比值(忽略液接电位).
比值(忽略液接电位).
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“下列电池Pt Sn4+,Sn2+溶液II标准甘汞电极30℃时…”相关的问题
更多“下列电池Pt Sn4+,Sn2+溶液II标准甘汞电极30℃时…”相关的问题
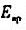 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。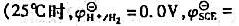
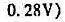
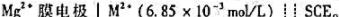 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。 离子电极测定,当把1.00×10-2mol/L的NaClO3溶液加入被测试液中的体积分别为0、1.00mL、2.00mL、3.00mL、4.00mL、5.00mL时,所测得的电池电位依次为-0.167V,-0.159V,-0.154V,-0.149V,-0.146V和-0.143V,求未知液中NaClO3的浓度。
离子电极测定,当把1.00×10-2mol/L的NaClO3溶液加入被测试液中的体积分别为0、1.00mL、2.00mL、3.00mL、4.00mL、5.00mL时,所测得的电池电位依次为-0.167V,-0.159V,-0.154V,-0.149V,-0.146V和-0.143V,求未知液中NaClO3的浓度。

















