 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应(1)的 =-2.2kJ·mol-1,反应(2)的
=-2.2kJ·mol-1,反应(2)的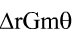 =-4.4kJ·mol-1,相同条件下两反应速率关系为( )。
=-4.4kJ·mol-1,相同条件下两反应速率关系为( )。
A.ν1>ν2
B.ν1<ν2
C.ν1=ν2
D.无法判断
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 =-2.2kJ·mol-1,反应(2)的
=-2.2kJ·mol-1,反应(2)的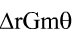 =-4.4kJ·mol-1,相同条件下两反应速率关系为( )。
=-4.4kJ·mol-1,相同条件下两反应速率关系为( )。A.ν1>ν2
B.ν1<ν2
C.ν1=ν2
D.无法判断
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应(1)的=-2.2kJ·mol-1,反应(2)的=-4.…”相关的问题
更多“反应(1)的=-2.2kJ·mol-1,反应(2)的=-4.…”相关的问题
A.1和-119.7kJ·mol-1
B.1和119.7kJ·mol-1
C.2和-119.7kJ·mol-1
D.2和119.7kJ·mol-1
已知NO(g)和NO2(g)的

(A) 33.2kJ·mol-1(B) 57.1kJ·mol-1
(C) 123.5kJ·mol-1(D) 90.3kJ·mol-1
有基元反应Cl(g)+H2(g)→HCl(g)+H(g),已知它们的摩尔质量和直径分别为
MCl=35.45g·mol-1,-1=2.016g·mol-1
dCl=0.20nm,
已知下列两个反应:
(1)2H2(g)+O2(g)=2H2O(1);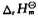 (298K)=-571.70kJ·mol-1
(298K)=-571.70kJ·mol-1
(2)2H2(g)+O2(g)=2H2O(g);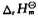 (298K)=-483.65kJ· mol-1
(298K)=-483.65kJ· mol-1
求298K时水的标准摩尔汽化热。
蔗糖水解反应
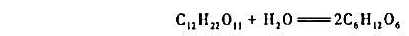
活化能Ea=110kJ·mol-1;298K是其半衰期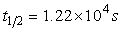 ,且
,且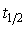 与反应物浓度无关。
与反应物浓度无关。
(1)求此反应的反应级数;
(2)写出气速率方程;
(3)求308K时的速率常数k。
A.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-11.46 kJ•mol-1
B.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-11.46 kJ·mol-1
C.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
D.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-57.3 kJ•mol-1
已知下列化学反应的标准摩尔反应焓变,求乙炔(C2H2,g)的标准摩尔生成焓 。
。
(1)C2H2(g)+5/2O2(g)→2CO2(g)+H2O(g) =-1246.2kJ·mol-1
=-1246.2kJ·mol-1
(2)C(s)+2H2O(g)→CO2(g)+2H2(g) =+90.9kJ·mol-1
=+90.9kJ·mol-1
(3)2H2O(g)→2H2(g)+O2(g)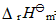 =+483.6kJ·mol-1
=+483.6kJ·mol-1
在100℃下,反应COCl2(g)===CO(g)+Cl2(g)的KΘ=8.1×10-9,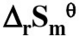 =125.6J·mol-1·K-1。计算:(1)100℃,总压力为200kPa时COCl2的离解度;(2)100℃下上述反应的
=125.6J·mol-1·K-1。计算:(1)100℃,总压力为200kPa时COCl2的离解度;(2)100℃下上述反应的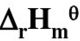 ;(3)总压力为200kPa,COCl2的解离度为0.1%时的温度。设△rCp,m=0。
;(3)总压力为200kPa,COCl2的解离度为0.1%时的温度。设△rCp,m=0。
A.-252.9 kJ·mol-1
B.+252.9 kJ·mol-1
C.-604.5 kJ·mol-1
D.+604.5 kJ·mol-1
A.的燃烧热大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀醋酸与稀NaOH溶液反应生成1 mol 水,放出57.3 kJ热量