题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应2HCl(g)=H2(g)+Cl2(g)的△fGθm =190.44 kJ·mol-1,则HCI(g)的△rGΘm为A.-95.22kJ·mol-1 B. +
反应2HCl(g)=H2(g)+Cl2(g)的△fGθm =190.44 kJ·mol-1,则HCI(g)的△rGΘm为
A.-95.22kJ·mol-1 B. +95.22kJ·mol-1
C.-190.44kJ·mol-1 D. +190.44kJ·mol-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“反应2HCl(g)=H2(g)+Cl2(g)的△fGθm =…”相关的问题
更多“反应2HCl(g)=H2(g)+Cl2(g)的△fGθm =…”相关的问题
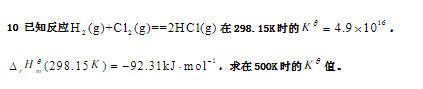
 (快速平衡)
(快速平衡) =-184.6kJ·mol-1,由此可知HCl(g)的标准摩尔生成焓为( )。
=-184.6kJ·mol-1,由此可知HCl(g)的标准摩尔生成焓为( )。 对于反应:H2(g)+Cl2(g)===2HCl(g),下列说法正确的是()。
对于反应:H2(g)+Cl2(g)===2HCl(g),下列说法正确的是()。