 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.1mol·L-1Fe2+和0.01mol·L-1Fe3+组成的电极,其电极电势是______。(=0.77V)
用0.1mol·L-1Fe2+和0.01mol·L-1Fe3+组成的电极,其电极电势是______。(
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.1mol·L-1Fe2+和0.01mol·L-1Fe3+组成的电极,其电极电势是______。(
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用0.1mol·L-1Fe2+和0.01mol·L-1Fe3…”相关的问题
更多“用0.1mol·L-1Fe2+和0.01mol·L-1Fe3…”相关的问题
用O.02 tool·L-1KMn04溶液滴定0.1 mol·L-1:Fe2+溶液(2)用0.002 mol·L-1KMnO4溶液滴定0.01 mol·L-1Fe2+溶液上述两种情况下其滴定突跃将是()。
A.一样大
B.(1)>(2)
C.(2)>(1)
D.缺电位值,无法判断
欲除去0.1mol·L-1Fe2+溶液中含有的杂质Fe3+。控制pH在什么范围内,可使Fe3+以Fe(OH)3形式沉淀完全,而Fe2+不产生沉淀。已知:Ksp(Fe(OH)3)≈10-38,Ksp(Fe(OH)2)≈10-15。(提示:当Fe3+的浓度小于1×10-5mol·L-1时,可认为沉淀完全)
 和
和 表示,则
表示,则 /
/ 为( )
为( )A.10
B.100
C.0.1
D.0.01
移取25.00mLHCOOH和HAc的混合溶液,以酚酞为指示剂,用0.1000mol·L-1NaOH滴定至终点,消耗35.20mL。另取25.00mL混合试液,调节为强碱性,加入50.00mL0.01500mol·L-1KMnO4溶液将HCOOH氧化至CO2。酸化溶液,加入0.1000mol·L-1Fe2+溶液25.00mL,然后再用上述KMnO4溶液滴定,用去32.00mL,计算混合液中HCOOH和HAc的浓度各为多少?
移取20.00mL HCOOH和HAc的混合溶液,以0.1000mol·L-1NaOH溶液滴定至终点时,共消耗25.00mL。另取上述溶液20.00mL,准确加入0.02500mol·L-1KMnO4强碱性溶液50.00mL,使其反应完全后,调至酸性,加入0.20000mol·L-1Fe2+标准溶液40.00mL,将剩余的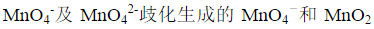 全部还原至Mn2+,剩余的Fe2+溶液用上述KMnO4标准溶液滴定,至终点时消耗24.00mL。计算试液中HCOOH和HAc的浓度。
全部还原至Mn2+,剩余的Fe2+溶液用上述KMnO4标准溶液滴定,至终点时消耗24.00mL。计算试液中HCOOH和HAc的浓度。
A.EΘ+0.0592/2
B.EΘ+0.0592
C.EΘ-0.0592
D.EΘ-00592/2
A.0.01mol/L盐酸, 红色
B.0.1mol/L盐酸,绿色
C.0.01mol/L盐酸,黄色
D.0.1mol/L盐酸,黄色