 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在298K时的标准状态下,MnO2和盐酸反应能否制得Cl2?如果改用12molL-1的浓盐酸呢?(设其他物质仍处在标准状态)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在298K时的标准状态下,MnO2和盐酸反应能否制得Cl2?…”相关的问题
更多“在298K时的标准状态下,MnO2和盐酸反应能否制得Cl2?…”相关的问题
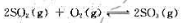
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
298K时,已知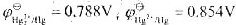 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
已知下述反应298K时的热效应:
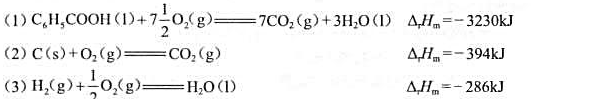 求C6H5COOH(1)的标准生成热ΔHƟm。
求C6H5COOH(1)的标准生成热ΔHƟm。
25℃时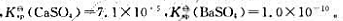 则沉淀转化反应:
则沉淀转化反应: 在25℃时的标准平衡常数
在25℃时的标准平衡常数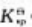 =()。在25℃标准状态下,上述反应方向为()。
=()。在25℃标准状态下,上述反应方向为()。
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
已知298K时下述电池的电动势为1.362V,
(Pt)H2(pθ)|H2SO4(aq)|Au2O3=Au(s)
又知H2O(g)的ΔrGmθ=-228.6kJ·mol-1,该温度下水的饱和蒸汽压为3167Pa,
求在298K时氧气的逸度为多少才能使Au2O3与Au呈平衡?