 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
柠檬酸为三元弱酸,用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。A、
柠檬酸为三元弱酸,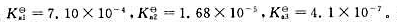 用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
A、1个
B、2个
C、3个
D、无突跃
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
柠檬酸为三元弱酸,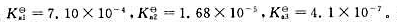 用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
A、1个
B、2个
C、3个
D、无突跃
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“柠檬酸为三元弱酸,用NaOH标准溶液滴定0.1000mol·…”相关的问题
更多“柠檬酸为三元弱酸,用NaOH标准溶液滴定0.1000mol·…”相关的问题
用NaOH溶液滴定某弱酸HA时(两者浓度相同),当滴定至一半时,溶液的pH值为5.00;当滴定至化学计量点时,溶液的pH值为8.00;当滴定至200%时溶液pH值为12.00。则该酸(HA)的pKa值是()。
A.5.00
B.8.00
C.12.00
D.7.00
测定一工业硫酸的含量,取样1.1250g,稀释成250mL。摇匀后移取25.00mL,用浓度为0.1340mol·L-1的NaOH标准溶液滴定,消耗15.40mL。求该工业硫酸中硫酸的质量分数。
A.用直接法配制NaOH标准溶液
B.把K2Cr2O7标准溶液装在碱式滴定管中
C.把Na2S2O3标准溶液装在棕色细口瓶中
D.用EDTA标准溶液滴定Ca2+时,滴定速度要快
A.1:3
B.3:1
C.1:2
D.1:1
在下列溶液中,能用NaOH标准溶液直接滴定的是(Et≤0.1%)()。
A.0.I mol·L-1 NH2OH·HCl(盐酸羟胺) [pKb(NH2OH)=8.04]
B.0.1 mol·L-1 NH4C1(氯化铵) [pKa(NH4C1)=9.26]
C.0.1 mol·L-1(CH2)6N4(六次甲基四胺) [pKb(CH2)6 N4=8.85]
D.0.1 mol·L-1 C5H5N(吡啶) [pKb(C5H5N)=8.87]
以下叙述正确的是()。
A.用HCl滴定NaOH,选PP为指示剂的终点误差为正值
B.NaOH滴定HCl,选MO为指示剂的终点误差是正值
C.用蒸馏法测NH4+,若采用HCl吸收NH3,以NaOH返滴定至pH为7.0,终点误差为正值
D.蒸馏法测NH4+,若采用H3BO3吸收NH3,以HCl滴定至MO变色,终点误差为负值
A.6.7~8.7
B.6.7~10.7
C.7.7~8.7
D.7.7~10.7
(4分)下列0.10 mol·L-1的弱酸或弱碱能否用酸碱滴定法直接滴定?为什么?
(1)苯甲酸(pKθa=4.21)
(2)六次甲基四胺(pKθb=8.85)
A.NaHCO3
B.NaHCO3、Na2CO3
C.Na2CO3
D.Na2CO3、NaOH
用0.1000 mol·L-1NaOH标准溶液滴定0.10 mol·L-1HCI和0.10 mol·L-1H3P04混合溶液时,可能有(8) 个滴定突跃。已知:H3P04的Kθa1 =7.5×10-3,Kθa2=6.2×10-8,Kθa3=2.2×10-13。