 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于多数溶液,在汽液平衡时,易发挥组分在汽相中的浓度总是()液相中的浓度。
A.大于
B.小于
C.等于
D.小于或等于
 答案
答案
A、大于
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.大于
B.小于
C.等于
D.小于或等于
 答案
答案
A、大于
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于多数溶液,在汽液平衡时,易发挥组分在汽相中的浓度总是()…”相关的问题
更多“对于多数溶液,在汽液平衡时,易发挥组分在汽相中的浓度总是()…”相关的问题
对于完全互溶的二元系苯(B)和氯仿(C),在343K,0.1MPa下汽液平衡(VLE)常数K值为KB=0.719,KC=1.31。试计算:
A.利用不同物质的组分在涂有固定液的固定相中溶解度的差异,从而在两相中有不同的分配系数,当混合物质通过色谱柱时,使单一物质组分得到分离,即挥发-溶解-再溶解-再挥发直至分离;
B.利用不同物质的组分在涂有固定液的固定相中溶解度的差异,从而在两相中有不同的分配系数,当混合物质通过色谱柱时,使单一物质组分得到分离,即溶解-再溶解-挥发-再挥发直至分离;
C.利用不同物质的组分在涂有固定液的固定相中溶解度的差异,从而在两相中有不同的分配系数,当混合物质通过色谱柱时,使单一物质组分得到分离,即溶解-挥发-再溶解-再挥发直至分离;
D.利用不同物质的组分在涂有固定液的固定相中溶解度的差异,从而在两相中有不同的分配系数,当混合物质通过色谱柱时,使单一物质组分得到分离,即挥发-溶解-再挥-再溶解发直至分离。
已知化合物A、B属于同系物,其蒸气压如下:
温度/℃ | p_A^S/kPa | p_B^S/kPa |
65.6 | 80.0 | 66.66 |
93.3 | 133.32 | 126.66 |
假设化合物组成理想溶液,计算:79.4℃,xA=0.500时,达到汽液平衡时组分A的气相摩尔分数和系统的总压。已知:Clausius-Clapeyron方程为。
汽相组成.
已知:Wilson方程的二元交互作用能量参数为

纯组分的摩尔体积: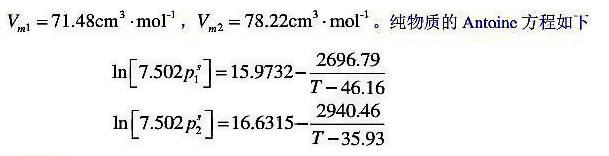
Psi的单位为kPa,T单位K.
.试求此溶液的泡点温度及其平衡的汽相组成.假设苯甲苯混合物可作理想体系处理,该两组分的Antoine(安托因)方程如下
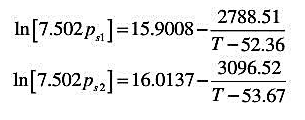
Psi的单位为kPa,T单位K.
110℃时,水(1)-正丁醇(2)液液平衡数据为x'1=0.9788,x"2=0.6759。试计算汽相的组成y及总压p。
已知饱和蒸气压为:
活度系数采用Van Laar方程计算:
其中A、B为活度系数方程参数。
101.325kPa下水(A)-醋酸(B)系统的气-液平衡数据如下。
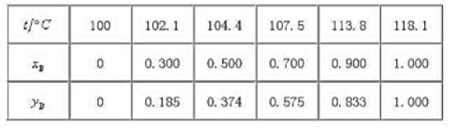
(1)画出气-液平衡的温度-组成图。
(2)从图上找出组成为xB=0.800的气相的泡点。
(3)从图上找出组成为yB=0.800的液相的露点。
(4)105.0°C时气-液平衡两相的组成是多少?
(5)9kg水与30kg醋酸组成的系统在105.0°C达到平衡时,气一液两相的质量各位多少?
101.325kPa下水(A)-醋酸(B)系统的气-液平衡数据如下:

(1)断出气-液中衡的温度一组成图;
(2)从图上找出组成为xB=0.800的液相的泡点;
(3)从图上:找出组成为yB=0.800的气相的露点;
(4)105.0℃时气-液平衡两相的组成是多少?
(5)9kg水与30kg醋酸组成的系统在105.0℃达到平衡时,气、液网相的质量各为多少?
A.称量时使用的砝码锈蚀
B.移液管转移溶液之后残留量稍有不同
C.滴定管刻度未经校正
D.读取滴定管读数时,最后一位数字估计不准
E.在沉淀重量分析中,样品中的非被测组分被共沉淀
对于异构化反应A====B,在400K下可快速建立平衡。在该温度下它们的蒸气压为:
