 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
NaOH溶液标签浓度为L,该溶液从空气中吸收了少量的CO2,现以酚酞为指示剂,用标准HCl溶液标定,标定结果比标签浓度()。
A.高;
B.低;
C.不变
D.无法确定
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.高;
B.低;
C.不变
D.无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“NaOH溶液标签浓度为L,该溶液从空气中吸收了少量的CO2,…”相关的问题
更多“NaOH溶液标签浓度为L,该溶液从空气中吸收了少量的CO2,…”相关的问题
A.OH-相同
B.NaOH和NH3OH的浓度相同(mol/L)
C.两物质的pKb相同
D.两个滴定的pH突跃范围相同
用NaOH溶液滴定某弱酸HA时(两者浓度相同),当滴定至一半时,溶液的pH值为5.00;当滴定至化学计量点时,溶液的pH值为8.00;当滴定至200%时溶液pH值为12.00。则该酸(HA)的pKa值是()。
A.5.00
B.8.00
C.12.00
D.7.00
某氯化物溶液100ml,今移取25.00ml溶液3份,用浓度为(0.1057±0.0002)mo/L(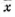 ±S)的AgNO3溶液滴定,分别消耗AgNO3溶液35.15ml,35.22ml和35.19ml,按偶然误差传递规则计算该氯化物溶液中Cl-的量(mmol/L)。
±S)的AgNO3溶液滴定,分别消耗AgNO3溶液35.15ml,35.22ml和35.19ml,按偶然误差传递规则计算该氯化物溶液中Cl-的量(mmol/L)。
A.5.62×10-10
B.3.2×10-10
C.8.4×10-9
D.7.1×10-8
已知M(NH3)42+的 为2.0、5.0、7.0、10.0; M(OH)42+的
为2.0、5.0、7.0、10.0; M(OH)42+的 为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?
为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?
A.偏低
B.偏高
C.无影响
D.不确定