 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知Fe3+的d电子成对能为358kJ·mol-1,由F-或CN-的八面体场形成配合
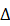 0(F-)=13961cm-1,
0(F-)=13961cm-1,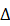 0(CN-)=34850cm-1,试由此判断:(1)[Fe(CN)6]3及[FeF6]3-的相对稳定性大小.(2)[Fe(CN)6]3-及[FeF6]3-的自旋状态及磁矩.(3)计算它们的晶体场稳定化能(不考虑电子之间的相互作用).
0(CN-)=34850cm-1,试由此判断:(1)[Fe(CN)6]3及[FeF6]3-的相对稳定性大小.(2)[Fe(CN)6]3-及[FeF6]3-的自旋状态及磁矩.(3)计算它们的晶体场稳定化能(不考虑电子之间的相互作用).
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
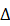 0(F-)=13961cm-1,
0(F-)=13961cm-1,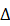 0(CN-)=34850cm-1,试由此判断:(1)[Fe(CN)6]3及[FeF6]3-的相对稳定性大小.(2)[Fe(CN)6]3-及[FeF6]3-的自旋状态及磁矩.(3)计算它们的晶体场稳定化能(不考虑电子之间的相互作用).
0(CN-)=34850cm-1,试由此判断:(1)[Fe(CN)6]3及[FeF6]3-的相对稳定性大小.(2)[Fe(CN)6]3-及[FeF6]3-的自旋状态及磁矩.(3)计算它们的晶体场稳定化能(不考虑电子之间的相互作用).
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知Fe3+的d电子成对能为358kJ·mol-1,由F-或…”相关的问题
更多“已知Fe3+的d电子成对能为358kJ·mol-1,由F-或…”相关的问题
已知配离子[CoCl 2 (en) 2 ] + 的磁矩为零,则配离子的空间构型为________。该配离子的中心离子 d 轨道分裂能比电子成对能________,d 电子的排布方式为___________。
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
相同中心离子与不同配体形成八面体配合物时,中心离子 d 轨道的分裂能△ o 与电子成对能(P)的关系是:强配体场中△ o ________P;在弱配体场中△ o ________P。
n=3的电子,其l值可能为()。
A.0,1,2
B.1,2,3
C.0,±1,±2
D.0,1,2,3
准确称取铁矿石试样0.5000g,用酸溶解后加入SnCl2,使Fe3+还原为Fe2+,滴定Fe2+消耗24.50mLKMnO4标准溶液滴定,已知1mL.KMnO4相当于0.01260gH2C2O4·2H2O,(1)矿样中Fe及Fe2O3的质量分数各为多少?(2)取市售双氧水3.00mL,稀释定容于250.00mL,从中取出20.00mL试液,需用上述溶液KMnO421.18mL滴定至终点,计算每100.0mL市售双氧水所含H2O2的质量.
(电子科技大学2007年硕士研究生入学考试试题)已知某负反馈系统的开环对数渐近幅频特性如图5-54所示,设系统开环放大系数为K,图中ω2=4,且ω=0.1处的幅值为40dB。
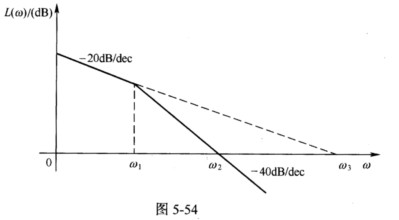 (1)证明:ω22=ω1ω3。 (2)设系统为最小相位系统,求相角裕量γ。
(1)证明:ω22=ω1ω3。 (2)设系统为最小相位系统,求相角裕量γ。