 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于密闭容器中的可逆反应2HI(g) = I2(g)+H2(g),下列叙述能够说明已达平衡状态的是()
A.气体密度保持不变
B.压强保持不变的状态
C.断裂2mol H-I键的同时生成1mol I-I键
D.混合气体的颜色不再变化时
 答案
答案
D、混合气体的颜色不再变化时
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.气体密度保持不变
B.压强保持不变的状态
C.断裂2mol H-I键的同时生成1mol I-I键
D.混合气体的颜色不再变化时
 答案
答案
D、混合气体的颜色不再变化时
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于密闭容器中的可逆反应2HI(g) = I2(g)+H2(…”相关的问题
更多“对于密闭容器中的可逆反应2HI(g) = I2(g)+H2(…”相关的问题
A.HI、I2、H2的浓度相等时
B.混合气体的颜色不变化时
C.混合气体的总压强不变化时
D.HI、I2、H2的反应速率之比为2:1:1时
500℃时,可逆反应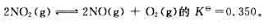 如果将一定量NO2(g)充入一不含任何气体的密闭容器中,平衡时测得NO(g)的分压34.4kPa.则NO2(g)的初始分压为().O2(g)的平衡分压为(),NO(g)的平衡分压为,NO(g)的平衡解离度为()。
如果将一定量NO2(g)充入一不含任何气体的密闭容器中,平衡时测得NO(g)的分压34.4kPa.则NO2(g)的初始分压为().O2(g)的平衡分压为(),NO(g)的平衡分压为,NO(g)的平衡解离度为()。
A.生成1molCO的同时生成1molH2
B.容器中物质的总质量不发生变化
C.n(H2O):n(H2)=1 :1
D.v逆(H2O)=v正(CO)
A.等于5s
B.等于10s
C.大于10s
D.小于10s
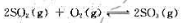
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
A.容器中,SO2、O2与SO3共存且浓度相等
B.容器中,SO2、O2与SO3的物质的量之比为2︰1︰2
C.正反应生成SO3的速率等于逆反应生成O2的速率
D.反应容器内混合气体平均相对分子质量不随时间的变化而改变
A.体系的压强不再发生变化
B.v正(CO)=v逆(H2O)
C.生成n mol CO的同时生成n mol H2
D.1 mol H—H键断裂的同时断裂2 mol H—O键
A.③、④、⑤、⑥
B.②、③、④、⑥
C.①、③、④、⑤
D.①、③、④、⑥
A.密闭容器中充入1 mol N2和3 mol H2可生成2 mol NH3
B.一定条件下,可逆反应达到平衡状态,该反应就达到了这一条件下的最大限度
C.对于任何反应增大压强,化学反应速率均增大
D.化学平衡是一种动态平衡,条件改变,原平衡状态不会被破坏
A.若单位时间内生成xmol NO的同时,消耗xmol NH3,则反应达到平衡状态
B.达到化学平衡时,若增大容器的体积,正反应速率减小,逆反应速率增大
C.达到化学平衡时,若升高温度,正反应速率增大,逆反应速率也增大
D.化学反应反应速率关系2υ正(NH3) = 3υ正(H2O)