 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列关于饱和食盐水的用途及装置设计正确的是()
A.-模拟工业制纯碱
B.-制乙酸乙酯实验中接受产物
C.-除去氯化氢中的氯气
D.-实验室制乙炔
 答案
答案
D、-实验室制乙炔
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.-模拟工业制纯碱
B.-制乙酸乙酯实验中接受产物
C.-除去氯化氢中的氯气
D.-实验室制乙炔
 答案
答案
D、-实验室制乙炔
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列关于饱和食盐水的用途及装置设计正确的是()”相关的问题
更多“下列关于饱和食盐水的用途及装置设计正确的是()”相关的问题
某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原Cu0呢?他们设计实验制取氮气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式()。
(2有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的()(填“能”或“否”)。理由是()。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性: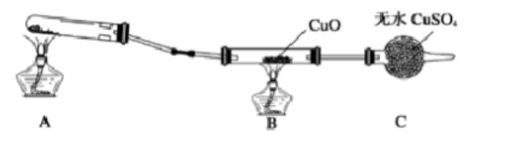 ⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
⑴该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是:()。
(2)利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与Cu0反应的化学方程式()。
(三)问题讨论:
有同学认为:NH3与Cu0反应生成的红色物质中可能含有Cu20.已知:Cu20是一种碱性氧化物;在酸性溶液中,Cu'的稳定性差(Cu+→Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu0:()。
A.为了加快反应速率可用饱和食盐水代替水反应
B.此反应是放热反应
C.为了除去杂质气体,除了用硫酸铜外还可用氢氧化钠溶液
D.反应中不需加碎瓷片作沸石
A.氯化钠溶解度变小
B.溶液依然饱和,溶质质量分数不变
C.食盐水在空气中变质而不能继续使用
D.水分蒸发,溶质的质量分数变大
A.海水淡化的方法中,蒸馏法成本最低
B.海水中含量最多的两种元素为Na元素和Cl元素
C.可以通过电解饱和食盐水的方式获取金属钠和氯气
D.从溴化钾中获取单质溴发生了氧化还原反应
A.Na2CO3溶液处理水垢中的CaSO4
B.水壶中的水垢可用白醋浸泡除去
C.实验室用饱和食盐水除氯气中氯化氢时,饱和食盐水变浑浊
D.实验室用氢氧化钠吸收氯气