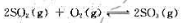题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
二级可逆反应动力学 在催化剂(HCl)的作用下,乙酸甲酯于25℃发生如下水解反应: 反应在25℃的平衡常数为0.2
二级可逆反应动力学
在催化剂(HCl)的作用下,乙酸甲酯于25℃发生如下水解反应:
CH3COOCH3+H2O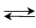 CH3COOH+CH3O 反应在25℃的平衡常数为0.22,乙酸甲酯和水的初始浓度分别为1.15mol/L和48.76mol/L。实验测得当反应进行到1h的时候,有34.92%的乙酸甲酯发生了水解。若正逆反应均为二级,试求反应速度常数k和k'。
CH3COOH+CH3O 反应在25℃的平衡常数为0.22,乙酸甲酯和水的初始浓度分别为1.15mol/L和48.76mol/L。实验测得当反应进行到1h的时候,有34.92%的乙酸甲酯发生了水解。若正逆反应均为二级,试求反应速度常数k和k'。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“二级可逆反应动力学 在催化剂(HCl)的作用下,乙酸甲酯于2…”相关的问题
更多“二级可逆反应动力学 在催化剂(HCl)的作用下,乙酸甲酯于2…”相关的问题
 R+S
R+S