 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在含有0.010mol·L-1Zn2+,0.10mol·L-1HAc和0.050mol·L-1NaAc的溶液中
,不断通入H2S(g)使之饱和,问沉淀出ZnS之后,溶液中残留的Zn2+是多少?(虽然是缓冲系统,pH的微小变化也会引起Zn2+浓度的变化,这一点是要考虑的.)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在含有0.010mol·L-1Zn2+,0.10mol·L-…”相关的问题
更多“在含有0.010mol·L-1Zn2+,0.10mol·L-…”相关的问题
下列溶液中能否产生沉淀?(1)0.020mol·L-1BaCl2溶液与0.010mol·L-1Na2CO3溶液等体积混合;(2)0.050mol·L-1MgCl2溶液与0.10mol·L-1氨水等体积混合;(3)在0.10mol·L-1HAc和0.10mol·L-1FeCl2混合溶液中通人H2S气体达饱和(约0.10mol·L-1).
度的影响).已知锌氨配离子的各级累积稳定常数为: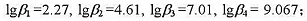 NH4+的离解常数为Ka=10-9.25.
NH4+的离解常数为Ka=10-9.25.
298.15K时,Mg(OH)2的标准溶度积常数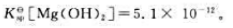 试计算:
试计算:
(1)Mg(OH)2在水中的溶解度:
(2)Mg(OH)2饱和溶液中的Mg2+、OH-的浓度和溶液的pH;
(3)Mg(OH)2在0.010mol·L-1NaOH溶液中的溶解度;
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度。
250K时化学反应A+2B=2C速率和浓度的关系如下:

(1)写出反应的速率方程,并指出反应指数.
(2)求该反应的速率常数.
(3)求出当c(A)=0.010mol·L-1,c(B)=0.020mol·L-1时的反应速率.