 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列制配单质的反应中,化合物作还原剂的是()
A.锌和硫酸反应制配氢气
B.溴和碘化钠反应制配碘
C.在电炉中碳和二氧化硅反应制配硅
D.铝和二氧化锰反应冶炼锰
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.锌和硫酸反应制配氢气
B.溴和碘化钠反应制配碘
C.在电炉中碳和二氧化硅反应制配硅
D.铝和二氧化锰反应冶炼锰
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列制配单质的反应中,化合物作还原剂的是( )”相关的问题
更多“下列制配单质的反应中,化合物作还原剂的是( )”相关的问题
间接碘量法测定铜合金中铜含量,KI起的作用为()。
A.还原剂、沉淀剂、配合剂
B.还原剂、沉淀剂、催化剂
C.氧化剂、沉淀剂、指示剂
D.氧化剂、沉淀剂、催化剂
选择适当的还原剂,将下列化合物中的羰基还原成亚甲基.
(1)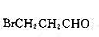 (2)
(2)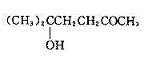 (3)
(3)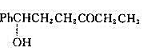
A.Cu+2AgN03=Cu(N03)2+2Ag
B.2Al+3H2S04=Al2(S04)3+3H2t
C.2Mg+C0
D.2Na202+2C02=2Na2C03+02
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
A.在氯化亚锡还原中,Sn2+离子数与99mTc原子数的比值应为103~106
B.Sn2+量太少还原反应不完全
C.Sn2+量太大易形成还原水解锝,产生放射性胶体
D.Sn2+量过大不会影响99mTc标记
E.氯化亚锡易氧化、水解,标记及药盒存放中应注意
试写出下列反应的化学方程式,并叙述实验现象:
(1)单质碘溶于在碘化钾溶液中;
(2)在碘化钾溶液中不断通入氯气,直至过量;
(3)少量硫粉与氯酸钾混合均匀后慢慢研磨;
(4)在硝酸汞溶液中逐滴加人碘化钾,直至过量;
(5)高碘酸在酸性条件下与二价锰离子反应;
(6)向次氯酸钠溶液中加入几滴硫酸锰。