 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,表明反应:A(g)+B(g) ⇌C(g)+D(g)已达平衡的是()
A.混合气体的压强
B.混合气体的密度
C.的物质的量浓度
D.气体的总物质的量
 答案
答案
C、的物质的量浓度
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.混合气体的压强
B.混合气体的密度
C.的物质的量浓度
D.气体的总物质的量
 答案
答案
C、的物质的量浓度
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,…”相关的问题
更多“在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,…”相关的问题
)和CO2(g)。当该分解反应达到平衡后,系统中共有压力不变的条件下将平衡系统中Na2CO3(s)除去·部分,化学平衡衡系统中的NaHCO3(s)全部除去,在其他条件不变时系统处于()。
在温度T时,CO和H2O在密闭容器内发生下列反应:
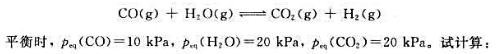
(1)此温度下该可逆反应的标准平衡常数;
(2)反应开始前反应物的分压;
(3)CO的平衡转化率。
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: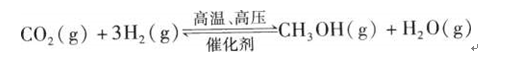
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
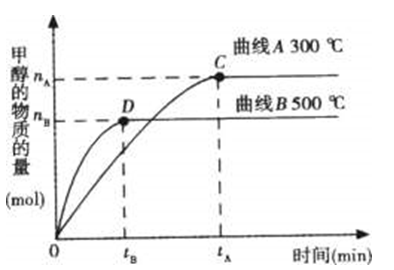
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
已知反应 在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
A.质量比为1∶9的H2和O2
B.质量比为3∶6的C和O2
C.质量比为1∶6的CH4和O2
D.质量比为7∶2的CO和O2
在一定温度下,反应物A(g)进行恒容反应,速率系数kA=2.0×10-3mol-1.dm.s-1,A(g)的初始浓度cA,D=0.05mol.dm-3。此反应的级数n=________,反应物A(g)的半衰期t1/2=______________。