 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有理想气体反应A(g)+B(g)=3C(g),在等温下维持体系总压不变,向体系中加入惰性气体,平衡()移动;若在恒温下将气体置于钢筒内加入惰性气体后平衡()移动。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有理想气体反应A(g)+B(g)=3C(g),在等温下维持体…”相关的问题
更多“有理想气体反应A(g)+B(g)=3C(g),在等温下维持体…”相关的问题
A.低温、高压
B.高温、高压
C.低温、低压
D.高温、低压
A.6.07x103;
B.6.07;
C.60.7;
D.607
工业生产SO2Cl2(1)有以下两种方法:
SO2(g)+C(g)=SO2Cl2(1)①
SO2(g)+2HCl(g)=SO2Cl2(1)+H2O(1)②
(1)请根据热力学数据计算说明,欲得到更大的转化率,应采用什么路线更好?
(2)对于②反应,增大体系温度,对反应有什么影响?
(3)求反应①在298K时的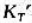
根据Le Chatelier原理,讨论下列反应:
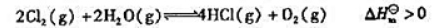
将Cl2,H2O(g),HCl(g),O2四种气休混合后,反应达到平衡时,下列左面的操作条件改变对右面各物理鼠的平衡数值有何影响(操作条件中没有注明的,是指温度不变和体积不变)?

在2L的容器中放入0.1mol的甲烷,封闭后加热到1273K,此时甲烷按CH4(g) C(s)+2H2(g)分解,测定容器内的压力为7.02bar,由于温度较高,容器内的气体可以视为理想气体。计算分解反应在1273K的化学平衡常数。
C(s)+2H2(g)分解,测定容器内的压力为7.02bar,由于温度较高,容器内的气体可以视为理想气体。计算分解反应在1273K的化学平衡常数。
A.一定量,一定组成的理想气体的绝热可逆过程;
B.等温等压,W'=0的任一过程
C.等温等压,W'=0的可逆过程
D.在-5℃,101.325kPa下过冷水的结冰过程
 2NH3(g)的反应,25dm3N2(g)与过量的H2(g)反应后,生成NH3(g)的体积是( )dm3。
2NH3(g)的反应,25dm3N2(g)与过量的H2(g)反应后,生成NH3(g)的体积是( )dm3。A.75
B.50
C.25
D.8.3
反应2Cl2(g)+2H2O(g)====4HCl(g)+O2(g)的
(A) 增加容器体积 (B) 降低温度 (C) 加入氧气 (D) 加入催化剂
某基元反应2A(g)+B(g)=C(g)+D(g)的初始分压PA=81.04 kPa,PB=60.78 kPa。当反应至PC=20.2 kPa时,反应速率大约是初始速率的
A.1/6 8.1/16 C.1/24 D.1/48